Organ Transplant
Research Lines
Content with Investigacion .
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
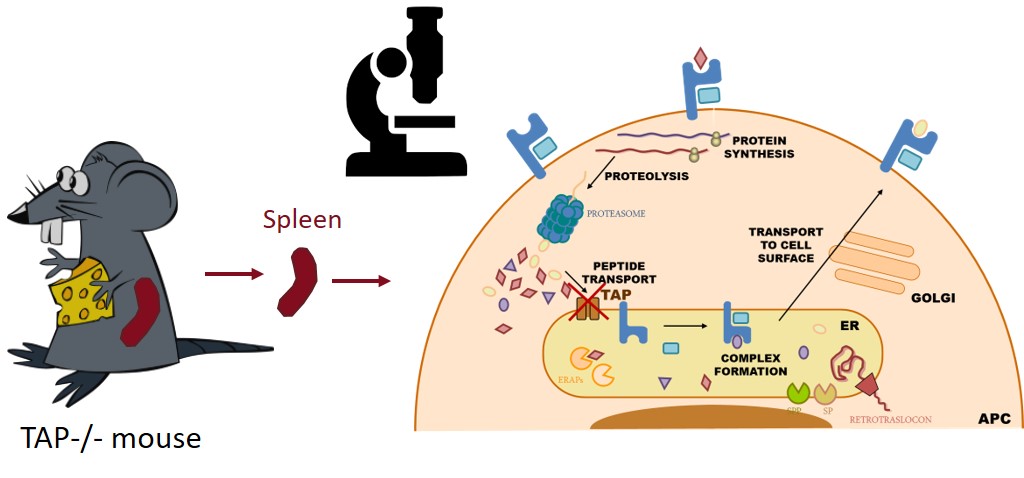
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
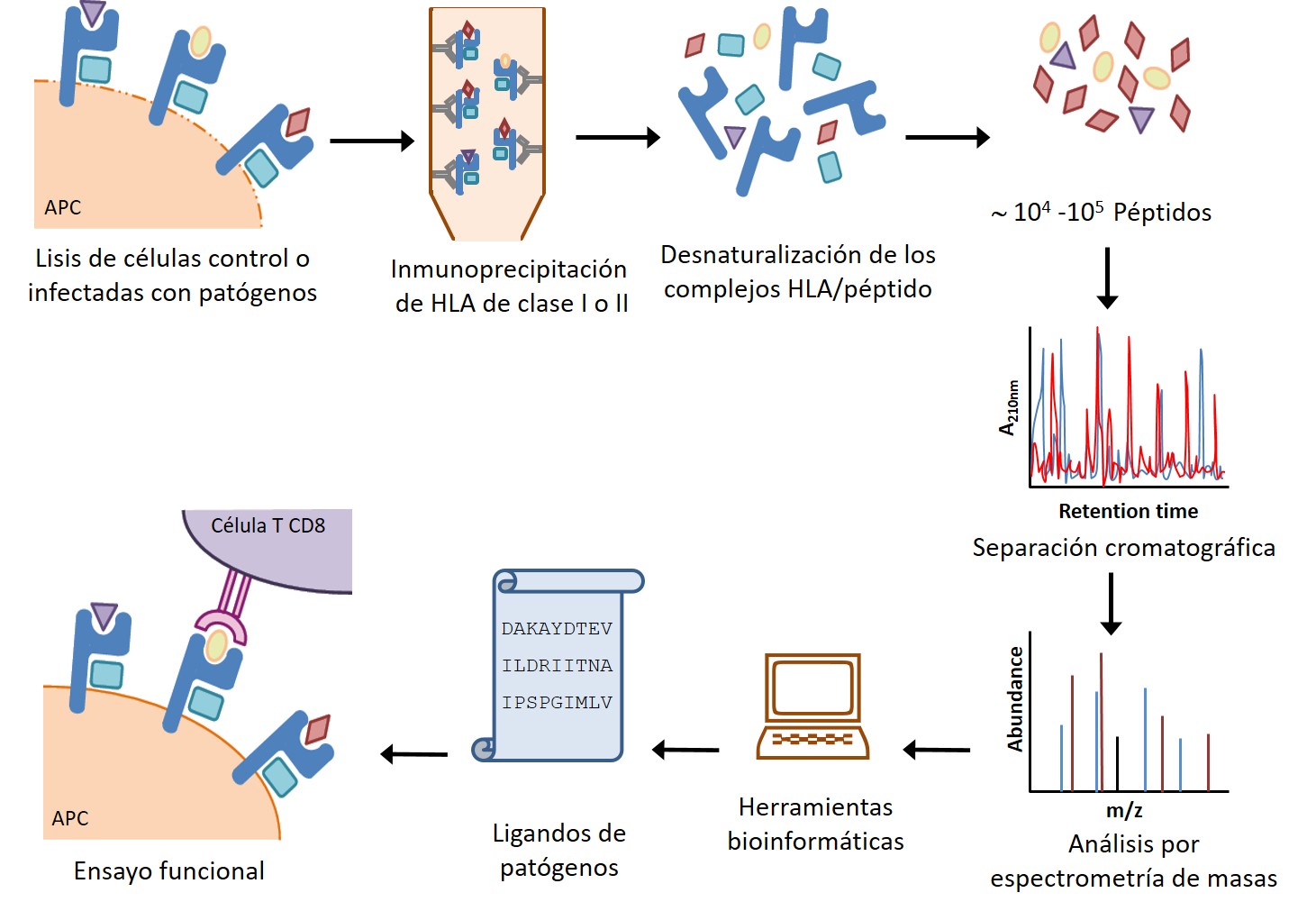
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
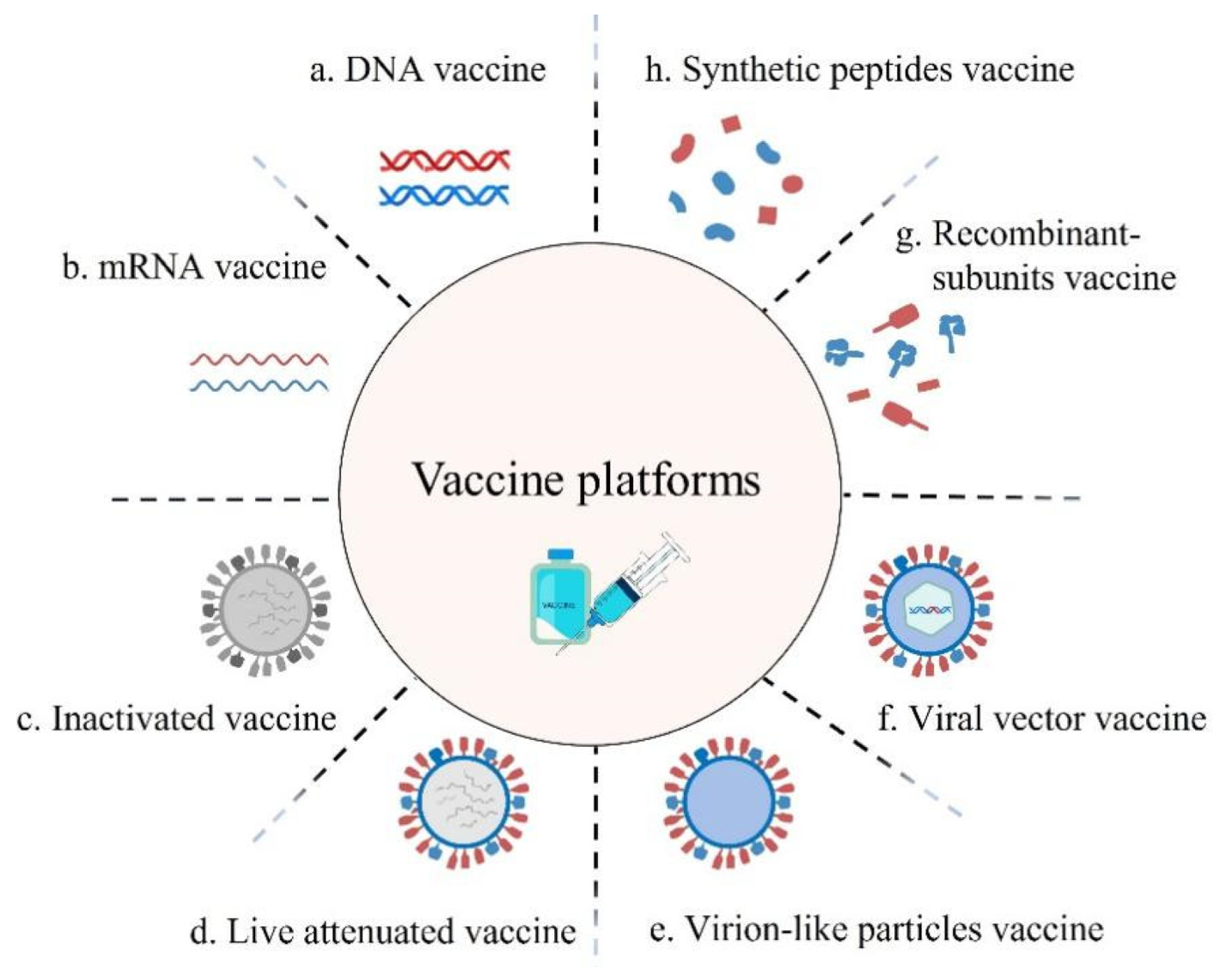
- * Generación de virus recombinantes como vectores vacunales.
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Phlebotomine sand fly survey in the focus of leishmaniasis of Madrid, Spain (2012–2014): seasonal dynamics, Leishmania infantum infection rates and blood meal preferences.
González E, Jiménez M, Hernández S, Martín-Martín I, Molina R. Phlebotomine sand fly survey in the focus of leishmaniasis of Madrid, Spain (2012–2014): seasonal dynamics, Leishmania infantum infection rates and blood meal preferences. Parasit Vectors 2017, 10:368.
PUBMED DOIMethods in Sand Fly Research
Molina R, Jiménez M, Alvar J, González E, Hernández-Taberna S, Martín-Martín Inés. 2017. Methods in Sand Fly Research (R. Molina, M. Jiménez & J. Alvar, edits.). Servicio de Publicaciones Universidad de Alcalá de Henares. ISBN: 978-84-16978-28-1
Factors associated with Leishmania asymptomatic infection: results from a cross-sectional survey in highland northern Ethiopia
Custodio E, Gadisa E, Sordo L, Cruz I, Moreno J, Nieto J, Chicharro C, Aseffa A, Abraham Z, Hailu T, Cañavate C. Factors associated with Leishmania asymptomatic infection: results from a cross-sectional survey in highland northern Ethiopia. PLoS Negl Trop Dis. 2012;6(9):e1813.
PUBMED DOICytokine Release Assays as Tests for Exposure to Leishmania, and for Confirming Cure from Leishmaniasis, in Solid Organ Transplant Recipients.
Carrillo E, Carrasco-Antón N, López-Medrano F, Salto E, Fernández L, San Martín JV, Alvar J, Aguado JM, Moreno J. Cytokine Release Assays as Tests for Exposure to Leishmania, and for Confirming Cure from Leishmaniasis, in Solid Organ Transplant Recipients. PLoS Negl Trop Dis. 2015 Oct 23;9(10):e0004179.
PUBMED DOIChemotactic Protein 1 in Plasma from Soluble Leishmania Antigen-Stimulated Whole Blood as a Potential Biomarker of the Cellular Immune Response to Leishmania infantum
Ibarra-Meneses AV, Sanchez C, Alvar J, Moreno J, Carrillo E. Monocyte Chemotactic Protein 1 in Plasma from Soluble Leishmania Antigen-Stimulated Whole Blood as a Potential Biomarker of the Cellular Immune Response to Leishmania infantum. Front Immunol. 2017 Sep 29;8:1208.
PUBMED DOICytokines and chemokines measured in dried SLA-stimulated whole blood spots for asymptomatic Leishmania infantum and Leishmania donovani infection.
Ibarra-Meneses AV, Mondal D, Alvar J, Moreno J, Carrillo E. Cytokines and chemokines measured in dried SLA-stimulated whole blood spots for asymptomatic Leishmania infantum and Leishmania donovani infection. Sci Rep. 2017 Dec 8;7(1):17266.
PUBMED DOICellular Markers of Active Disease and Cure in Different Forms of Leishmania infantum-Induced Disease.
Botana L, Matía B, San Martin JV, Romero-Maté A, Castro A, Molina L, Fernandez L, Ibarra-Meneses A, Aguado M, Sánchez C, Horrillo L, Chicharro C, Nieto J, Ortega S, Ruiz-Giardin JM, Carrillo E, Moreno J. Cellular Markers of Active Disease and Cure in Different Forms of Leishmania infantum-Induced Disease. Front Cell Infect Microbiol. 2018 Nov 13;8:381.
PUBMED DOICarroll MW et al. Temporal and spatial analysis of the 2014-2015 Ebola virus outbreak in West Africa. Nature.
Carroll MW et al. Temporal and spatial analysis of the 2014-2015 Ebola virus outbreak in West Africa. Nature. 2015 Aug 6;524(7563):97-101. doi: 10.1038/nature14594. Epub 2015 Jun 17. PMID: 26083749.
Fernandez-Garcia MD, Meertens L, Chazal M, Hafirassou ML, Dejarnac O, Zamborlini A, Despres P, Sauvonnet N, Arenzana-Seisdedos F, Jouvenet N, Amara A. Vaccine and Wild-Type Strains of Yellow Fever Virus Engage Distinct Entry Mechanisms and Differentially Stimulate Antiviral Immune Responses.
Fernandez-Garcia MD, Meertens L, Chazal M, Hafirassou ML, Dejarnac O, Zamborlini A, Despres P, Sauvonnet N, Arenzana-Seisdedos F, Jouvenet N, Amara A. Vaccine and Wild-Type Strains of Yellow Fever Virus Engage Distinct Entry Mechanisms and Differentially Stimulate Antiviral Immune Responses. mBio. 2016 Feb 9;7(1):e01956-15. doi: 10.1128/mBio.01956-15. PMID: 26861019; PMCID:PMC4752603.
Identification and whole-genome characterization of a recombinant Enterovirus B69 isolated from a patient with Acute Flaccid Paralysis in Niger, 2015
Fernandez-Garcia MD, Majumdar M, Kebe O, Ndiaye K, Martin J. Identification and whole-genome characterization of a recombinant Enterovirus B69 isolated from a patient with Acute Flaccid Paralysis in Niger, 2015. Sci Rep. 2018 Feb 1;8(1):2181. doi: 10.1038/s41598-018-20346-9. PMID: 29391547; PMCID: PMC5795009.
Majumdar M, Sharif S, Klapsa D, Wilton T, Alam MM, Fernandez-Garcia MD, Rehman L, Mujtaba G, McAllister G, Harvala H, Templeton K, Mee ET, Asghar H, Ndiaye K, Minor PD, Martin J. Environmental Surveillance Reveals Complex Enterovirus Circulation Patterns in Human Populations. Open Forum Infect Dis. 2018
Majumdar M, Sharif S, Klapsa D, Wilton T, Alam MM, Fernandez-Garcia MD, Rehman L, Mujtaba G, McAllister G, Harvala H, Templeton K, Mee ET, Asghar H, Ndiaye K, Minor PD, Martin J. Environmental Surveillance Reveals Complex Enterovirus Circulation Patterns in Human Populations. Open Forum Infect Dis. 2018 Oct 1;5(10):ofy250. doi: 10.1093/ofid/ofy250. PMID: 30377626; PMCID: PMC6201154.
Fernandez-Garcia MD, Majumdar M, Kebe O, Fall AD, Kone M, Kande M, Dabo M, Sylla MS, Sompare D, Howard W, Faye O, Martin J, Ndiaye K. Emergence of Vaccine-Derived Polioviruses during Ebola Virus Disease Outbreak, Guinea, 2014-2015.
Fernandez-Garcia MD, Majumdar M, Kebe O, Fall AD, Kone M, Kande M, Dabo M, Sylla MS, Sompare D, Howard W, Faye O, Martin J, Ndiaye K. Emergence of Vaccine-Derived Polioviruses during Ebola Virus Disease Outbreak, Guinea, 2014-2015. Emerg Infect Dis. 2018 Jan;24(1):65-74. doi: 10.3201/eid2401.171174. PMID:29260690; PMCID: PMC5749474.
Tarragó, D.; Mateos, M.-L.; Avellón, A.; Pérez-Vázquez, M.-D.; Tenorio, A.2004
Tarragó, D.; Mateos, M.-L.; Avellón, A.; Pérez-Vázquez, M.-D.; Tenorio, A.2004. Quantitation of Cytomegalovirus DNA in Cerebrospinal Fluid and Serum Specimens from AIDS Patients Using a Novel Highly Sensitive Nested Competitive PCR and the Cobas Amplicor CMV Monitor™ Journal of Medical Virology. 72-2, pp.249-256. ISSN 01466615. 10. Tarragó, D.; Quereda, C.; Tenorio, A.2003. Different cytomegalovirus glycoprotein B genotype distribution in serum and cerebrospinal fluid specimens determined by a novel multiplex nested PCR Journal of Clinical Microbiology. 41-7, pp.2872-2877. ISSN 00951137.
Fernandez-Garcia, Maria Dolores (AC); Kebe, Ousmane; Fall, Aichatou D.; Dia, Hamet; Diop, Ousmane M.; Delpeyroux, Francis; Ndiaye, Kader. 2016.
Fernandez-Garcia, Maria Dolores (AC); Kebe, Ousmane; Fall, Aichatou D.; Dia, Hamet; Diop, Ousmane M.; Delpeyroux, Francis; Ndiaye, Kader. (1/ 7). 2016. Enterovirus A71 Genogroups C and E in Children with Acute Flaccid Paralysis, West Africa EMERGING INFECTIOUS DISEASES. 22-4, pp.753-755. ISSN 1080-6040.
Molecular epidemiology of coxsackievirus B3 infection in Spain, 2004-2015.
K Calderón, M Díaz-de Cerio, C Muñoz-Almagro, N Rabella, I Martínez-Rienda, A Moreno-Docón, G Trallero, M Cabrerizo*. Molecular epidemiology of coxsackievirus B3 infection in Spain, 2004-2015. Arch Virol 161: 1365-1370 (2016).
PUBMED DOIDevelopment and Evaluation of a Serological Assay for the Diagnosis of Tuberculosis in Alpacas and Llamas.
Development and Evaluation of a Serological Assay for the Diagnosis of Tuberculosis in Alpacas and Llamas. Infantes-Lorenzo, Jose A.; Whitehead, Claire E.; Moreno, Inmaculada; et ál..FRONTIERS IN VETERINARY SCIENCE Volumen: 5 Número de artículo: 189 Fecha de publicación: AUG 13 2018
PUBMED DOIInfluence of the Microenvironment in the Transcriptome of Leishmania infantum Promastigotes: Sand Fly versus Culture
Influence of the Microenvironment in the Transcriptome of Leishmania infantum Promastigotes: Sand Fly versus Culture. Alcolea, Pedro J.; Alonso, Ana; Dominguez, Mercedes; et ál..PLOS NEGLECTED TROPICAL DISEASES Volumen: 10 Número: 5 Número de artículo: e0004693 Fecha de publicación: MAY 2016
PUBMED DOIContent with Investigacion .
-

Sara Vázquez Ávila
Técnico de Laboratorio
Obtuve mi título como Técnico de Laboratorio Clínico y Biomédico en el año 2020 y en el 2021obtuve el Grado Superior de Anatomía Patológica y Citodiagnóstico. Trabajé en el Centro Andaluz de Biología Molecular y Medicina Regenerativa (Sevilla) y en el Departamento de Farmacología de la Facultad de Medicina (Universidad Complutense de Madrid). Actualmente soy Técnico de Laboratorio en el Laboratorio de Helmintos del CNM (ISCIII).
-
Maria Jesús Perteguer Prieto
Investigadora Titular, Jefa de grupo
-

Javier Sotillo Gallego
Científico Titular
ORCID code: 0000-0002-1443-7233
En el año 2011 obtuve mi título de doctor “cum laude” por la Universidad de Valencia. Durante mi etapa postdoctoral en la James Cook University en Australia (2012-2019) me especialicé en estudiar las interacciones parásito-hospedador usando diferentes técnicas ómicas. En 2019 volví España y comencé a trabajar en el Laboratorio de Helmintos del CNM (ISCIII) primero como Investigador Miguel Servet y más adelante como Investigador Ramón y Cajal. Actualmente soy Científico Titular en el mismo laboratorio.
-

Ana Hernández González
Laboral Fijo Doctor
ORCID code: 0000-0001-6762-8175
Licenciada en Biología y doctora en Enfermedades Tropicales por la Universidad de Salamanca. Puestos ocupados con anterioridad: investigadora predoctoral en el IRNASA-CSIC (contrato JAE predoc), investigadora postdoctoral en el CNM (contrato Sara Borrell) e investigadora contratada como técnico superior en el CNM (RICET). Actualmente, personal Laboral Fijo Doctor en el laboratorio de Helmintos del CNM.
-

Esther Rodríguez Pérez
Técnico de Laboratorio
ORCID code: 0000-0002-3680-7733
Obtuve mi título como Graduada en Biología Sanitaria en el año 2015 y en el año 2019 obtuve el Grado Superior de Laboratorio de Diagnóstico Clínico. De 2019 a 2022 trabajé en el Museo Nacional de Ciencias Naturales (MNCN-CSIC), en el Departamento de Biogeoquímica y Ecología Microbiana. Actualmente trabajo como Técnico de Laboratorio en el Laboratorio de Helmintos del CNM (ISCIII).
-

Lourdes Castro Companioni
Ayudante de Investigación
ORCID code: 0009-0003-2746-4067
Bióloga sanitaria graduada en la Universidad de Alcalá de Henares (UAH), con master de Microbiología y Salud pública en la UAH en colaboración con el ISCIII.
List of staff
Additional Information
Induction of allograft tolerance remains a goal to be achieved in organ transplantation. Most therapeutic strategies focus on inhibition of the adaptive immune system, but recent data demonstrate that allogeneic recognition of myeloid cells initiates transplant rejection. Therapies targeting myeloid cells “in vivo” represent a potential target to induce immunological tolerance, but remain clinically unexplored.
Our laboratory uses a revolutionary nanoimmunotherapy of high-density lipoprotein (HDL) nanoparticles loaded with rapamycin (mTORi-HDL) that prevents epigenetic modifications associated with trained immunity, a recently discovered functional state of macrophages. Using an experimental mouse transplant model, our results demonstrate that the administration of this immunotherapy with mTORi-HDL prevents the immune response and promotes tolerance to the transplanted organ.
Our laboratory shows a multidisciplinary research approach articulated in three different objectives to evaluate the clinical relevance and therapeutic effects of immunotherapy in preparation for a clinical trial in organ transplantation. The general objectives will be aimed at confirming the identification of trained immunity as a biomarker and analytical value to predict the risk of rejection in transplant patients under three conditions: prolonged periods of ischemic reperfusion (IRI) (objective 1), allosensitization (objective 2) and infection (objective 3).
Induction of allograft tolerance remains a goal to be achieved in organ transplantation. Most therapeutic strategies focus on inhibition of the adaptive immune system, but recent data demonstrate that allogeneic recognition of myeloid cells initiates transplant rejection. Therapies targeting myeloid cells “in vivo” represent a potential target to induce immunological tolerance, but remain clinically unexplored.
Our laboratory uses a revolutionary nanoimmunotherapy of high-density lipoprotein (HDL) nanoparticles loaded with rapamycin (mTORi-HDL) that prevents epigenetic modifications associated with trained immunity, a recently discovered functional state of macrophages. Using an experimental mouse transplant model, our results demonstrate that the administration of this immunotherapy with mTORi-HDL prevents the immune response and promotes tolerance to the transplanted organ.
Our laboratory shows a multidisciplinary research approach articulated in three different objectives to evaluate the clinical relevance and therapeutic effects of immunotherapy in preparation for a clinical trial in organ transplantation. The general objectives will be aimed at confirming the identification of trained immunity as a biomarker and analytical value to predict the risk of rejection in transplant patients under three conditions: prolonged periods of ischemic reperfusion (IRI) (objective 1), allosensitization (objective 2) and infection (objective 3).