Organ Transplant
Research Lines
Content with Investigacion .
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
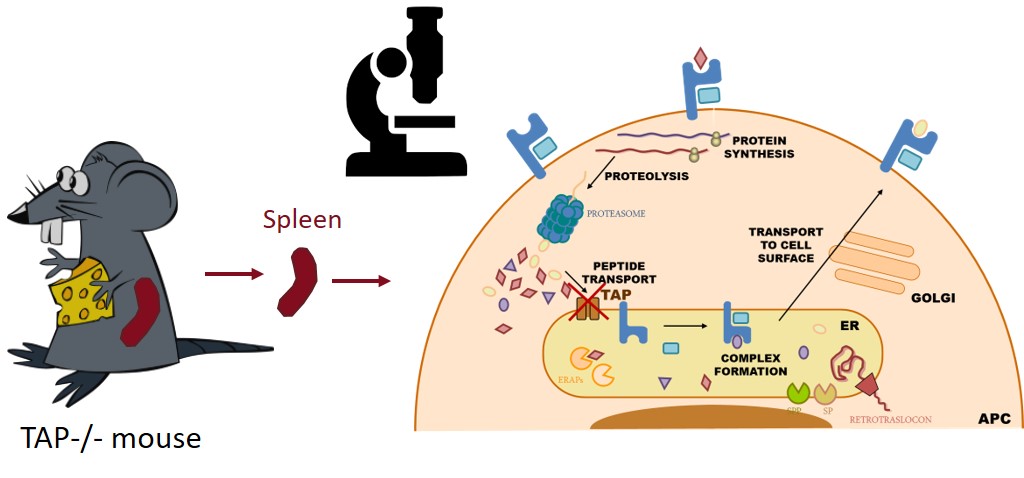
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
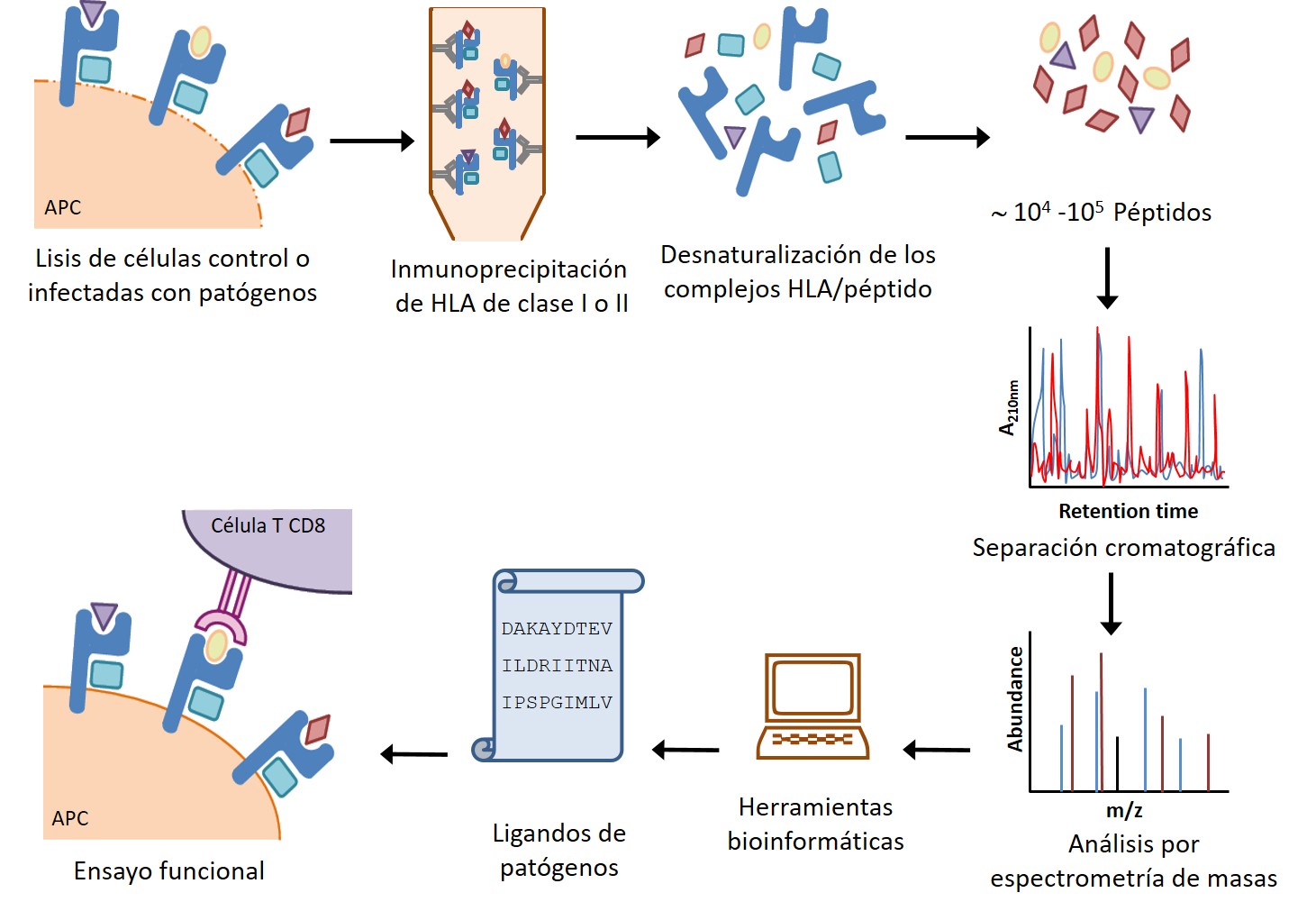
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
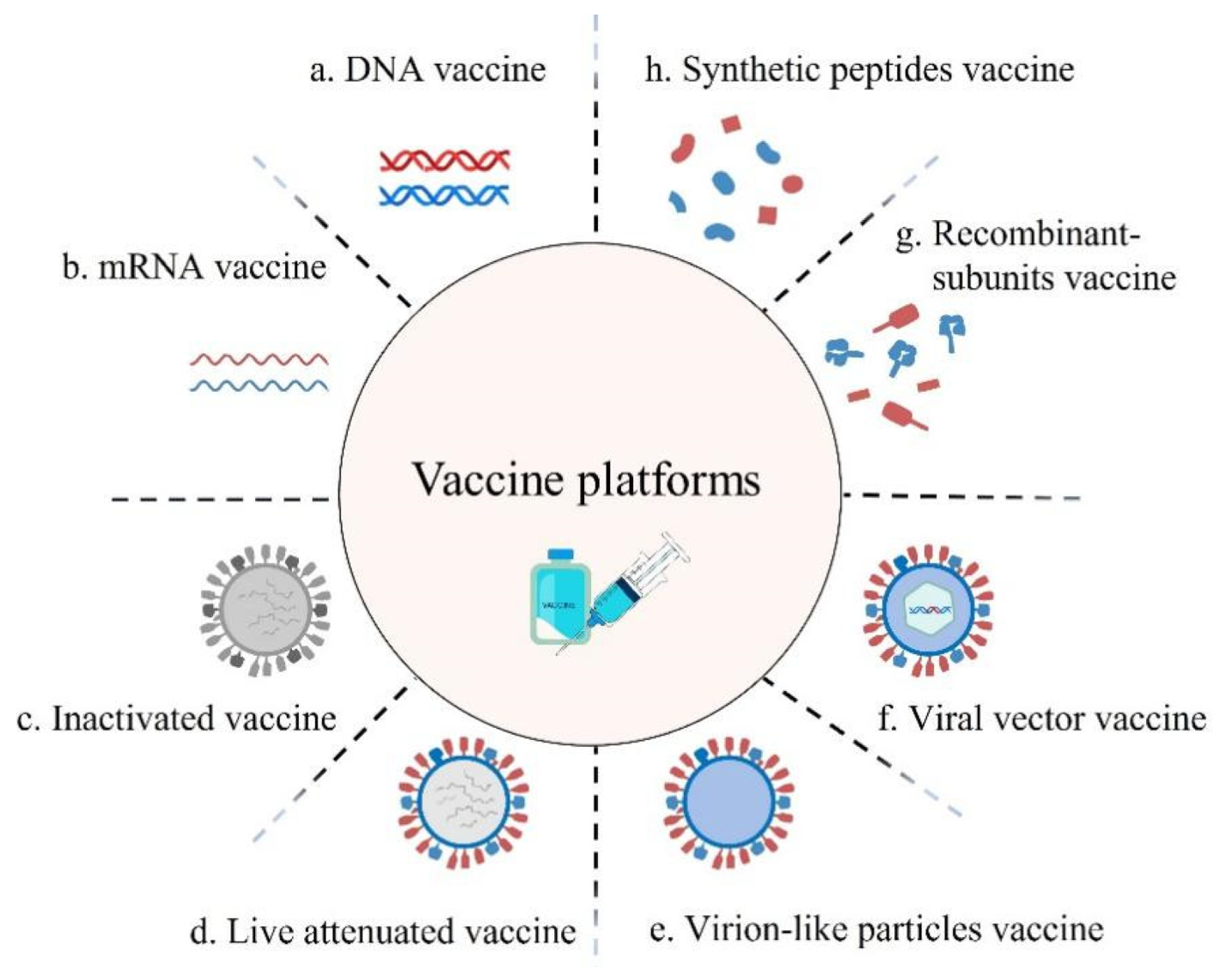
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Eva Orviz, Anabel Negredo, Oskar Ayerdi, Ana Vázquez, Ana Muñoz-Gomez, Sara Monzón, Petunia Clavo, Angel Zaballos, Mar Vera, Patricia Sánchez, Noemi Cabello, Pilar Jiménez, Jorge A Pérez-García, Sarai Varona, Jorge Del Romero, Isabel Cuesta, Alberto Delgado-Iribarren, Montse Torres, Iñigo Sagastagoitia, Gustavo Palacios, Vicente Estrada, Maria Paz Sánchez-Seco, Grupo Viruela del Simio Madrid CNM/ISCIII/HCSC/Sandoval.
Eva Orviz, Anabel Negredo, Oskar Ayerdi, Ana Vázquez, Ana Muñoz-Gomez, Sara Monzón, Petunia Clavo, Angel Zaballos, Mar Vera, Patricia Sánchez, Noemi Cabello, Pilar Jiménez, Jorge A Pérez-García, Sarai Varona, Jorge Del Romero, Isabel Cuesta, Alberto Delgado-Iribarren, Montse Torres, Iñigo Sagastagoitia, Gustavo Palacios, Vicente Estrada, Maria Paz Sánchez-Seco, Grupo Viruela del Simio Madrid CNM/ISCIII/HCSC/Sandoval. Monkeypox outbreak in Madrid (Spain): Clinical and virological aspects. J Infect. 2022 Jul 10;S0163-4453(22)00415-7. doi: 10.1016/j.jinf.2022.07.005.
DOIEuropean mitochondrial haplogroups are associated with CD4+ T-cell recovery in HIV-infected patients on combination antiretroviral therapy.
15. Guzmán-Fulgencio M; Berenguer J, Micheloud D, Fernández-Rodríguez A; García–Álvarez M, Jiménez-Sousa MA, Bellón JM, Campos Y, Cosin J, Aldámiz-Echevarría T, Catalán P, López JC, Resino S (*). European mitochondrial haplogroups are associated with CD4+ T-cell recovery in HIV-infected patients on combination antiretroviral therapy. J Antimicrob Chemoth 2013; 68 (10): 2349–2357 (A; FI= 5.44; D1, Infectious Diseases; JCR 2013). PMID: 23749950. DOI: 10.1093/jac/dkt206.
PUBMEDMaría Paz Sánchez-Seco, María José Sierra, Agustín Estrada-Peña, Félix Valcárcel, Ricardo Molina, Eva Ramírez de Arellano, Angeles Sonia Olmeda, Lucía García San Miguel, Maribel Jiménez, Luis J Romero, Anabel Negredo; Group for CCHFv Research. Widespread Detection of Multiple Strains of Crimean-Congo Hemorrhagic Fever Virus in Ticks, Spain.
María Paz Sánchez-Seco, María José Sierra, Agustín Estrada-Peña, Félix Valcárcel, Ricardo Molina, Eva Ramírez de Arellano, Angeles Sonia Olmeda, Lucía García San Miguel, Maribel Jiménez, Luis J Romero, Anabel Negredo; Group for CCHFv Research. Widespread Detection of Multiple Strains of Crimean-Congo Hemorrhagic Fever Virus in Ticks, Spain. Emerg Infect Dis. 2022 Feb;28(2):394-402. doi: 10.3201/eid2802.211308.
DOINegredo A, Sánchez-Ledesma M, Llorente F, Pérez-Olmeda M, Belhassen-García M, González-Calle D, Sánchez-Seco MP, Jiménez-Clavero MÁ. Retrospective Identification of Early Autochthonous Case of Crimean-Congo Hemorrhagic Fever, Spain, 2013
Negredo A, Sánchez-Ledesma M, Llorente F, Pérez-Olmeda M, Belhassen-García M, González-Calle D, Sánchez-Seco MP, Jiménez-Clavero MÁ. Retrospective Identification of Early Autochthonous Case of Crimean-Congo Hemorrhagic Fever, Spain, 2013. Emerg Infect Dis. 2021 Jun;27(6):1754-1756. doi: 10.3201/eid2706.204643.
DOIAdditional Information
Induction of allograft tolerance remains a goal to be achieved in organ transplantation. Most therapeutic strategies focus on inhibition of the adaptive immune system, but recent data demonstrate that allogeneic recognition of myeloid cells initiates transplant rejection. Therapies targeting myeloid cells “in vivo” represent a potential target to induce immunological tolerance, but remain clinically unexplored.
Our laboratory uses a revolutionary nanoimmunotherapy of high-density lipoprotein (HDL) nanoparticles loaded with rapamycin (mTORi-HDL) that prevents epigenetic modifications associated with trained immunity, a recently discovered functional state of macrophages. Using an experimental mouse transplant model, our results demonstrate that the administration of this immunotherapy with mTORi-HDL prevents the immune response and promotes tolerance to the transplanted organ.
Our laboratory shows a multidisciplinary research approach articulated in three different objectives to evaluate the clinical relevance and therapeutic effects of immunotherapy in preparation for a clinical trial in organ transplantation. The general objectives will be aimed at confirming the identification of trained immunity as a biomarker and analytical value to predict the risk of rejection in transplant patients under three conditions: prolonged periods of ischemic reperfusion (IRI) (objective 1), allosensitization (objective 2) and infection (objective 3).
Induction of allograft tolerance remains a goal to be achieved in organ transplantation. Most therapeutic strategies focus on inhibition of the adaptive immune system, but recent data demonstrate that allogeneic recognition of myeloid cells initiates transplant rejection. Therapies targeting myeloid cells “in vivo” represent a potential target to induce immunological tolerance, but remain clinically unexplored.
Our laboratory uses a revolutionary nanoimmunotherapy of high-density lipoprotein (HDL) nanoparticles loaded with rapamycin (mTORi-HDL) that prevents epigenetic modifications associated with trained immunity, a recently discovered functional state of macrophages. Using an experimental mouse transplant model, our results demonstrate that the administration of this immunotherapy with mTORi-HDL prevents the immune response and promotes tolerance to the transplanted organ.
Our laboratory shows a multidisciplinary research approach articulated in three different objectives to evaluate the clinical relevance and therapeutic effects of immunotherapy in preparation for a clinical trial in organ transplantation. The general objectives will be aimed at confirming the identification of trained immunity as a biomarker and analytical value to predict the risk of rejection in transplant patients under three conditions: prolonged periods of ischemic reperfusion (IRI) (objective 1), allosensitization (objective 2) and infection (objective 3).