Neisseria, Listeria and Bordetella
Research Lines
Content with Investigacion .
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
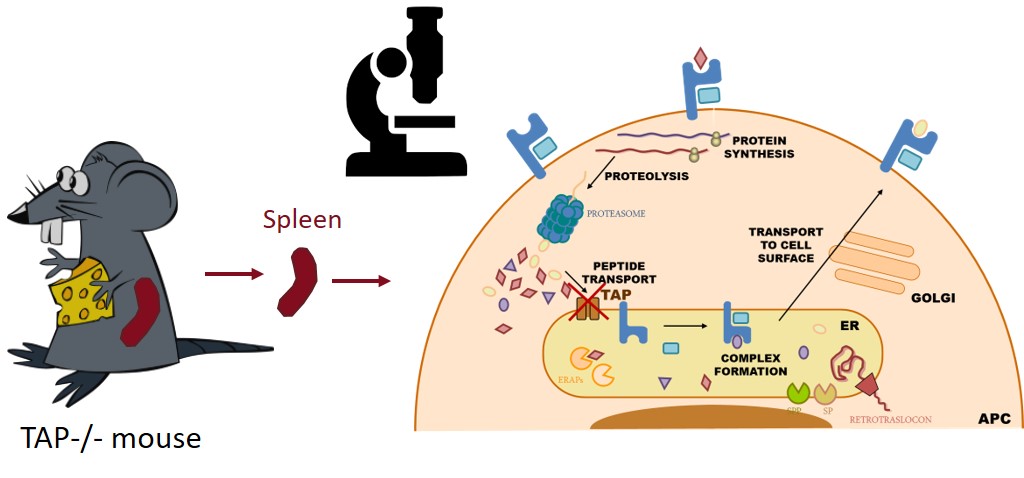
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
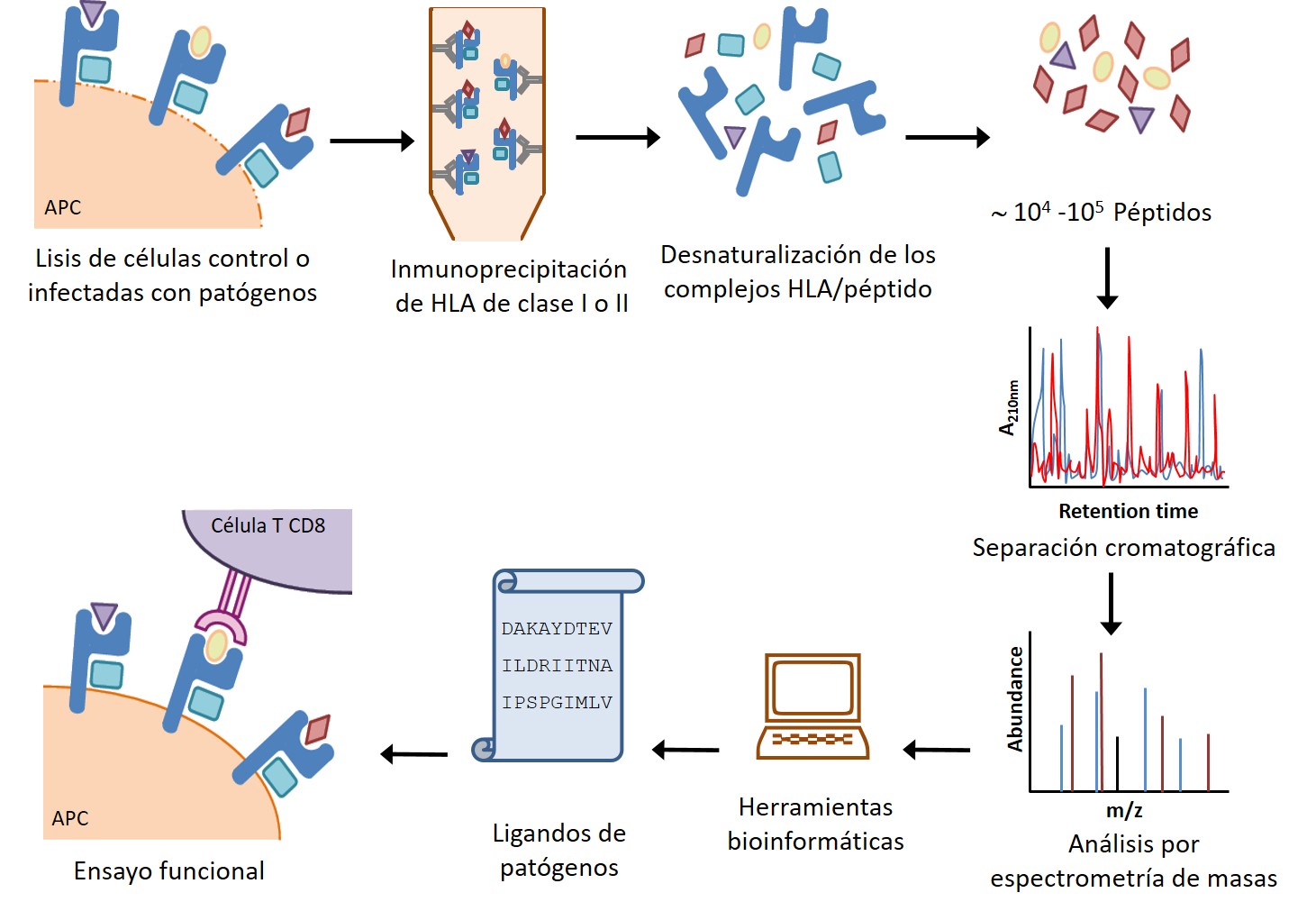
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

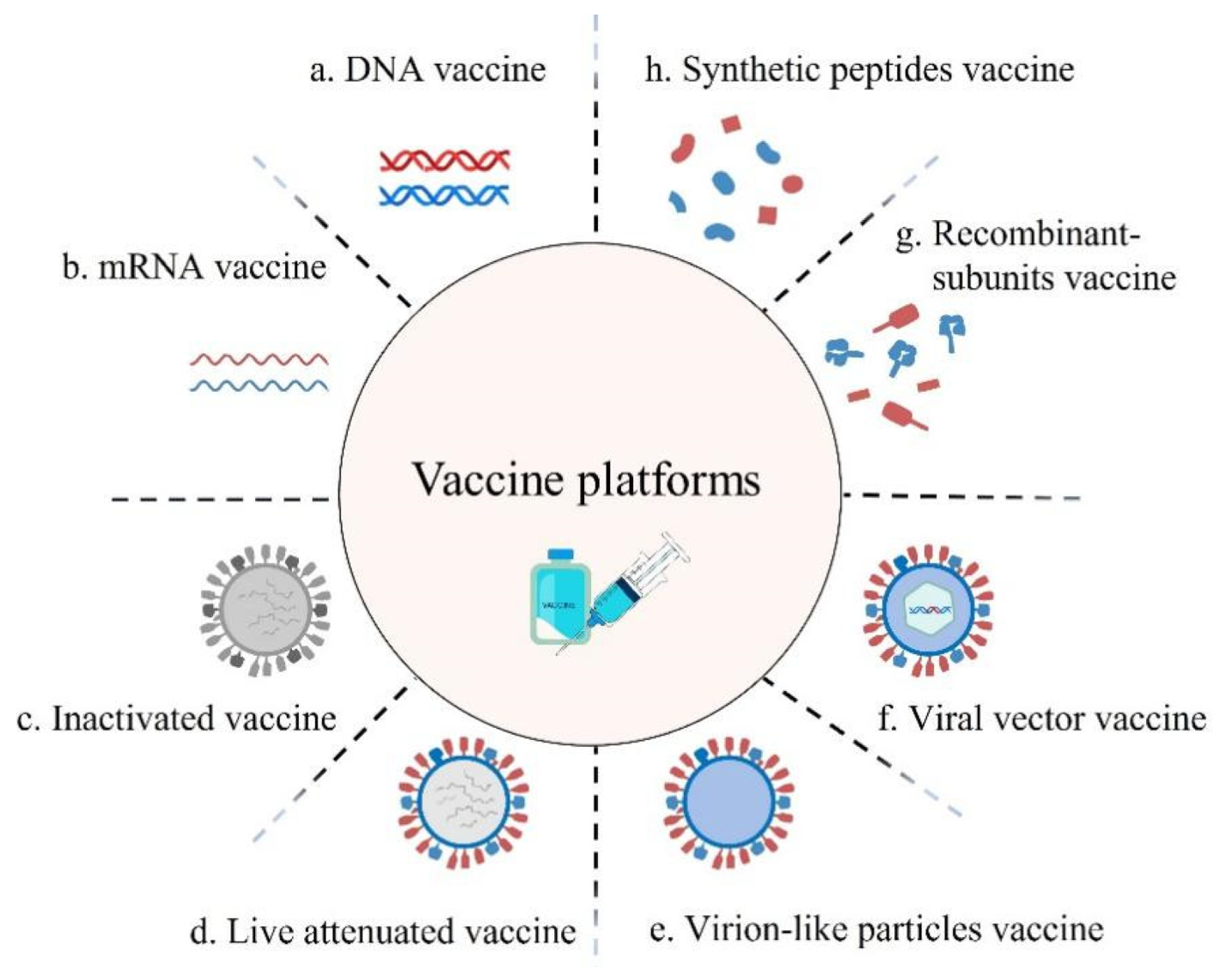
* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Alastruey-Izquierdo A, Alcazar-Fuoli L, Rivero-Menéndez O, Ayats J, Castro C, García-Rodríguez J, Goterris-Bonet L, Ibáñez-Martínez E, Linares-Sicilia MJ, Martin-Gomez MT, Martín-Mazuelos E, Pelaez T, Peman J, Rezusta A, Rojo S, Tejero R, Anza DV, Viñuelas J, Zapico MS, Cuenca-Estrella M; the FILPOP2 Project from GEMICOMED (SEIMC) and REIPI. Molecular Identification and Susceptibility Testing of Molds Isolated in a Prospective Surveillance of Triazole Resistance in Spain (FILPOP2 Study). Antimicrob Agents Chemother. 2018 Aug 27;62(9):e00358-18. doi: 10.1128/AAC.00358-18. PMID: 29941643; PMCID: PMC6125503.
Alastruey-Izquierdo A, Alcazar-Fuoli L, Rivero-Menéndez O, Ayats J, Castro C, García-Rodríguez J, Goterris-Bonet L, Ibáñez-Martínez E, Linares-Sicilia MJ, Martin-Gomez MT, Martín-Mazuelos E, Pelaez T, Peman J, Rezusta A, Rojo S, Tejero R, Anza DV, Viñuelas J, Zapico MS, Cuenca-Estrella M; the FILPOP2 Project from GEMICOMED (SEIMC) and REIPI. Molecular Identification and Susceptibility Testing of Molds Isolated in a Prospective Surveillance of Triazole Resistance in Spain (FILPOP2 Study). Antimicrob Agents Chemother. 2018 Aug 27;62(9):e00358-18. doi: 10.1128/AAC.00358-18. PMID: 29941643; PMCID: PMC6125503.
PUBMED DOIGonçalves SM, Lagrou K, Rodrigues CS, Campos CF, Bernal-Martínez L, Rodrigues F, Silvestre R, Alcazar-Fuoli L, Maertens JA, Cunha C, Carvalho A. Evaluation of Bronchoalveolar Lavage Fluid Cytokines as Biomarkers for Invasive Pulmonary Aspergillosis in At-Risk Patients. Front Microbiol. 2017 Nov 29;8:2362. doi:10.3389/fmicb.2017.02362. PMID: 29238334; PMCID: PMC5712575.
Gonçalves SM, Lagrou K, Rodrigues CS, Campos CF, Bernal-Martínez L, Rodrigues F, Silvestre R, Alcazar-Fuoli L, Maertens JA, Cunha C, Carvalho A. Evaluation of Bronchoalveolar Lavage Fluid Cytokines as Biomarkers for Invasive Pulmonary Aspergillosis in At-Risk Patients. Front Microbiol. 2017 Nov 29;8:2362. doi:10.3389/fmicb.2017.02362. PMID: 29238334; PMCID: PMC5712575.
PUBMED DOIAlcazar-Fuoli L, Buitrago M, Gomez-Lopez A, Mellado E. An alternative host model of a mixed fungal infection by azole susceptible and resistant Aspergillus spp strains. Virulence. 2015;6(4):376-84. doi: 10.1080/21505594.2015.1025192. PMID: 26065322; PMCID: PMC4601236.
Alcazar-Fuoli L, Buitrago M, Gomez-Lopez A, Mellado E. An alternative host model of a mixed fungal infection by azole susceptible and resistant Aspergillus spp strains. Virulence. 2015;6(4):376-84. doi: 10.1080/21505594.2015.1025192. PMID: 26065322; PMCID: PMC4601236.
PUBMED DOIAlcazar-Fuoli L, Cairns T, Lopez JF, Zonja B, Pérez S, Barceló D, Igarashi Y, Bowyer P, Bignell E. A modified recombineering protocol for the genetic manipulation of gene clusters in Aspergillus fumigatus. PLoS One. 2014 Nov 5;9(11):e111875. doi: 10.1371/journal.pone.0111875. PMID: 25372385; PMCID:PMC4221250.
Alcazar-Fuoli L, Cairns T, Lopez JF, Zonja B, Pérez S, Barceló D, Igarashi Y, Bowyer P, Bignell E. A modified recombineering protocol for the genetic manipulation of gene clusters in Aspergillus fumigatus. PLoS One. 2014 Nov 5;9(11):e111875. doi: 10.1371/journal.pone.0111875. PMID: 25372385; PMCID:PMC4221250.
PUBMED DOIBertuzzi M, Schrettl M, Alcazar-Fuoli L, Cairns TC, Muñoz A, Walker LA, Herbst S, Safari M, Cheverton AM, Chen D, Liu H, Saijo S, Fedorova ND, Armstrong-James D, Munro CA, Read ND, Filler SG, Espeso EA, Nierman WC, Haas H, Bignell EM. The pH-responsive PacC transcription factor of Aspergillus fumigatus governs epithelial entry and tissue invasion during pulmonary aspergillosis. PLoS Pathog. 2014 Oct 16;10(10):e1004413. doi: 10.1371/journal.ppat.1004413.
Bertuzzi M, Schrettl M, Alcazar-Fuoli L, Cairns TC, Muñoz A, Walker LA, Herbst S, Safari M, Cheverton AM, Chen D, Liu H, Saijo S, Fedorova ND, Armstrong-James D, Munro CA, Read ND, Filler SG, Espeso EA, Nierman WC, Haas H, Bignell EM. The pH-responsive PacC transcription factor of Aspergillus fumigatus governs epithelial entry and tissue invasion during pulmonary aspergillosis. PLoS Pathog. 2014 Oct 16;10(10):e1004413. doi: 10.1371/journal.ppat.1004413.
DOIYasmin S, Alcazar-Fuoli L, Gründlinger M, Puempel T, Cairns T, Blatzer M, Lopez JF, Grimalt JO, Bignell E, Haas H. Mevalonate governs interdependency of ergosterol and siderophore biosyntheses in the fungal pathogen Aspergillus fumigatus. Proc Natl Acad Sci U S A. 2012 Feb 21;109(8):E497-504. doi: 10.1073/pnas.1106399108. Epub 2011 Nov 21. PMID: 22106303; PMCID: PMC3286978.
Yasmin S, Alcazar-Fuoli L, Gründlinger M, Puempel T, Cairns T, Blatzer M, Lopez JF, Grimalt JO, Bignell E, Haas H. Mevalonate governs interdependency of ergosterol and siderophore biosyntheses in the fungal pathogen Aspergillus fumigatus. Proc Natl Acad Sci U S A. 2012 Feb 21;109(8):E497-504. doi: 10.1073/pnas.1106399108. Epub 2011 Nov 21. PMID: 22106303; PMCID: PMC3286978.
PUBMED DOIImpaired Cytotoxic Response in PBMCs From Patients With COVID-19 Admitted to the ICU: Biomarkers to Predict Disease Severity.
Impaired Cytotoxic Response in PBMCs From Patients With COVID-19 Admitted to the ICU: Biomarkers to Predict Disease Severity. Vigón L, Fuertes D, García-Pérez J, Torres M, Rodríguez-Mora S, Mateos E, Corona M, Saez-Marín AJ, Malo R, Navarro C, Murciano-Antón MA, Cervero M, Alcamí J, García-Gutiérrez V, Planelles V, López-Huertas MR, Coiras M (AC). Front Immunol. 2021 May 26;12:665329. doi: 10.3389/fimmu.2021.665329. eCollection 2021. PMID: 34122423.
PUBMED DOIIdentification of Immunological Parameters as Predictive Biomarkers of Relapse in Patients with Chronic Myeloid Leukemia on Treatment-Free Remission
Identification of Immunological Parameters as Predictive Biomarkers of Relapse in Patients with Chronic Myeloid Leukemia on Treatment-Free Remission. Vigón L, Luna A, Galán M, Rodríguez-Mora S, Fuertes D, Mateos E, Piris-Villaespesa M, Bautista G, San José E, Rivera-Torres J, Steegmann JL, de Ory F, Pérez-Olmeda M, Alcamí J, Planelles V, López-Huertas MR, García-Gutiérrez V, Coiras M (AC). J Clin Med. 2020 Dec 25;10(1):42. doi: 10.3390/jcm10010042. PMID: 33375572.
PUBMED DOIAdditional Information
The Neisseria, Listeria and Bordetella Unit provides support to the National Health System with the aim of improving the health and well-being of citizens, through the development and application of diagnostic and molecular characterization techniques, generating laboratory data essential for the surveillance of infectious diseases covered by the Unit, as well as maintaining lines of research for microbiological and immunological evaluation of vaccines, both in development and those available.
The Unit has 4 microbiological surveillance programs at the National Center for Microbiology: For invasive meningococcal disease, for gonococcal infection, for listeriosis and for whooping cough. Likewise, the Unit maintains extensive activity in international networks and consortia: it is part of the EU-Ibis consortium for the study of Meningococcal Disease, the EURO-GASP program for the study of antibiotic resistance in gonococcus, the European Listeria typing group network and the European network for Bordetella, all of them coordinated and financed in whole or in part by the ECDC.
The Unit constitutes the External Reference Laboratory for meningococci of the PAHO/WHO SIREVAII network. Thus, the active lines of research in the Unit respond to the objectives defined both by the support for the National Health System and by the international collaborative work in which it actively participates.
The Neisseria, Listeria and Bordetella Unit provides support to the National Health System with the aim of improving the health and well-being of citizens, through the development and application of diagnostic and molecular characterization techniques, generating laboratory data essential for the surveillance of infectious diseases covered by the Unit, as well as maintaining lines of research for microbiological and immunological evaluation of vaccines, both in development and those available.
The Unit has 4 microbiological surveillance programs at the National Center for Microbiology: For invasive meningococcal disease, for gonococcal infection, for listeriosis and for whooping cough. Likewise, the Unit maintains extensive activity in international networks and consortia: it is part of the EU-Ibis consortium for the study of Meningococcal Disease, the EURO-GASP program for the study of antibiotic resistance in gonococcus, the European Listeria typing group network and the European network for Bordetella, all of them coordinated and financed in whole or in part by the ECDC.
The Unit constitutes the External Reference Laboratory for meningococci of the PAHO/WHO SIREVAII network. Thus, the active lines of research in the Unit respond to the objectives defined both by the support for the National Health System and by the international collaborative work in which it actively participates.
The current director of CNM is Dr. José Miguel Rubio Muñoz.
Dr. José Miguel Rubio has a degree in Biological Sciences from the Universidad Autónoma de Madrid (1986) and a PhD in Biological Sciences from the same university (1992). He carried out his doctoral thesis at the Department of Genetics of the Universidad Autónoma de Madrid, as Associate Professor (1988-1989), and at the School of Biology of the University of East Anglia in Norwich, UK, as Senior Research Assistant (1989-1992).
During his postdoctoral period he obtained a grant from the European Commission within the Human Capital and Mobility Program to be carried out at the University of “La Sapienza” in Rome, Italy and the Institute of Molecular Biology and Biotechnology in Crete, Greece (1993-1994). Subsequently, he made a further stay funded by the WHO and the university itself at the Department of Entomology, Wageningen University, The Netherlands (1994-1996).
Since 1997 he has been a member of the Instituto de Salud Carlos III (ISCIII), where he joined the Department of Parasitology of the National Center of Microbiology, as an EU-INCO postdoctoral fellow and later with a grant from the Autonomous Community of Madrid (CAM). She was part of the founding group of the National Center for Tropical Medicine (2003-2006) and of the 24/7 Alerts and Emergencies Unit (2006-2018) and is currently Head of the Malaria and Emerging Parasitosis Unit of the National Microbiology Center and is part, as research staff, of the Center for Biomedical Research Network on Infectious Diseases (CIBERINFEC/ISCIII).
During his scientific career he has been Visiting Scientist at the Leonidas e Marie Dean Center (FIOCRUZ-AMAZONAS, Manaus, Brazil) and is an External Consultant of the Parasitology Departments of Cairo University (Egypt) and the Medical Research Center (MRC) of Kuala Lumpur (Malaysia). He also belongs or has belonged to different national and international committees: Member of the expert group for malaria control of the European Centre for Disease Control (ECDC) since 2011; Expert-Evaluator for health programs of the European Commission since 2004; Spanish Representative (commissioned by ISCIII and MSC) in the Technical Scientific Committee of the TDR (WHO) 2007-2008; Spanish Deputy Focal Point for microbiology at the European Centre for Disease Control (ECDC) from 2012 to 2020; and, member of the Research Ethics Committee of ISCIII until 2019.
In this period he has published more than 100 articles in international indexed journals, 10 book chapters and has been co-editor of two books in the area of malaria, tropical medicine and neglected diseases. He has participated in 58 competitively funded research projects, 20 of them international, having been the principal investigator in 8 national and 11 international projects as PI of the project or WP leader. In addition, he has led five agreements with companies. Currently he has been awarded four sexenios of research, being presented this year 2025 to the fifth. In the teaching field, he participates in different postgraduate programs in the areas of microbiology and parasitology, having directed seven doctoral theses and more than 20 Master's or Degree final projects, both nationally and internationally.
El laboratorio de Referencia e Investigación en Resistencia a Antibióticos ofrece una amplia cartera de servicios al Sistema Nacional de Salud, las cuales pueden solicitarse en cnm-laboratorios.isciii.es. Jefe del Laboratorio: Jesús Oteo Iglesias (Punto focal Nacional de Resistencia antibiótica).
Dispone de dos programas de Vigilancia oficiales y gratuitos que engloban los ensayos ofertados ya sea como aislamientos individuales o mediante estudio de brotes. El Laboratorio utiliza asimismo técnicas de PCR en tiempo real para la detección de genes de resistencia, estas técnicas se han adaptado a un formato multiplex que permite detectar varios genes en la misma reacción. En los últimos años se han incluido metodologías basadas en la secuenciación de genomas completos para el análisis de bacterias multiresistentes (WGS).
Programa de vigilancia de Haemophilus influenzae. Responsables: María Pérez Vázquez (Punto focal Nacional de Haemophilus influenzae) y Belén Aracil. Laboratorio encargado de la identificación, estudio de sensibilidad y análisis genotípico de aislados de Haemophilus influenzae, centrándose esencialmente en la patología invasiva debida este patógeno.
Programa de vigilancia de Resistencia a Antibióticos. Responsables: María Pérez Vázquez y Belén Aracil (Punto focal Nacional de Resistencia antibiótica). Laboratorio encargado de la identificación, el estudio de sensibilidad antibiótica, y el diagnóstico fenotípico y genotípico de los diferentes mecanismos de resistencia a antibióticos fundamentalmente en enterobacterias y gram-negativos no fermentadores y Enterococcus spp.
Estudio de brotes. Responsables: Belén Aracil y María Pérez Vázquez. El programa incluye la caracterización de brotes nosocomiales y clones emergentes de alto riesgo mediante diferentes técnicas moleculares (tabla resumen). Éstas, nos permiten realizar estudios filogenéticos con el fin de obtener una información detallada acerca la relación entre los diferentes aislados y su trazabilidad. El objetivo final es generar datos que se transfieren a los hospitales como ayuda para la prevención o control de la propagación del brote.
Acreditación y Calidad. Responsable: Belén Aracil. El laboratorio Referencia e Investigación en Resistencia a Antibióticos ha sido de los primeros en el ISCIII en la utilización de técnicas acreditadas por la Entidad Nacional de Acreditaciones (ENAC). Este laboratorio consiguió la primera acreditación homologada de técnicas diagnósticas en 2012, programa que ha sido ampliado, de manera que en la actualidad más de la mitad de las técnicas ofrecidas al Sistema Nacional de Salud están debidamente acreditadas por ENAC.
Técnicos responsables de las técnicas realizadas en el Laboratorio: Noelia Lara Fuella y Verónica Bautista Sánchez.
En la siguiente imagen se resumen las técnicas ofrecidas al Sistema Nacional de Salud.
| PROGRAMAS | NOMBRE CARTERA SERVICIO | PATÓGENO | DETERMINACIÓN, DETECCIÓN, ANÁLISIS | MÉTODOS |
|
Programa de vigilancia de Haemophilus Programa de vigilancia de resistencia a antibióticos. |
Identificación bacteriana |
Haemophilus sp. Enterobacterias, gram-negativos no fermentadores, Enterococcus spp |
Identificación bacteriana |
Bioquímicos MALDI TOF Secuenciación de RNAr |
| | Identificación capsular |
Haemophilus influenzae
|
Identificación capsular fenotípica y genotípica |
Aglutinación serológica en latex PCR ind/multiplex |
| | Determinación de Sensibilidad |
Haemophilus sp. Enterobacterias, gram-negativos no fermentadores, Enterococcus
|
Determinación de Sensibilidad |
Microdilución Tiras epsilon Kirby Bauer |
| | Métodos fenotípicos de detección de mecanismos de resistencia |
Enterobacterias, gram-negativos no fermentadores,
|
Métodos fenotípicos de detección de mecanismos de resistencia |
Discos y tabletas combinados con inhibidores Tiras combinadas Test de Hodge modificado CabaNP Inmunocromatografía CBP |
| | Métodos genotípicos de detección de mecanismos de resistencia |
Haemophilus sp. Enterobacterias, gram-negativos no fermentadores, Enterococcus
|
ADN, PCR y secuenciación |
PCR ind/multiplex Análisis comparativo de las secuencias |
| | Tipificación molecular/análisis filogenéticos |
Haemophilus sp. Enterobacterias, gram-negativos no fermentadores, Enterococcus
|
Corte enzimas de restricción, electroforesis ADN, PCR y secuenciación Preparación de librerías y secuenciación y análisis de genomas completos |
PFGE
MLST
WGS |