Legionella
Research Lines
Content with Investigacion .
Trasplante de órganos
null
Presentación y Regulación Inmunes
null
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
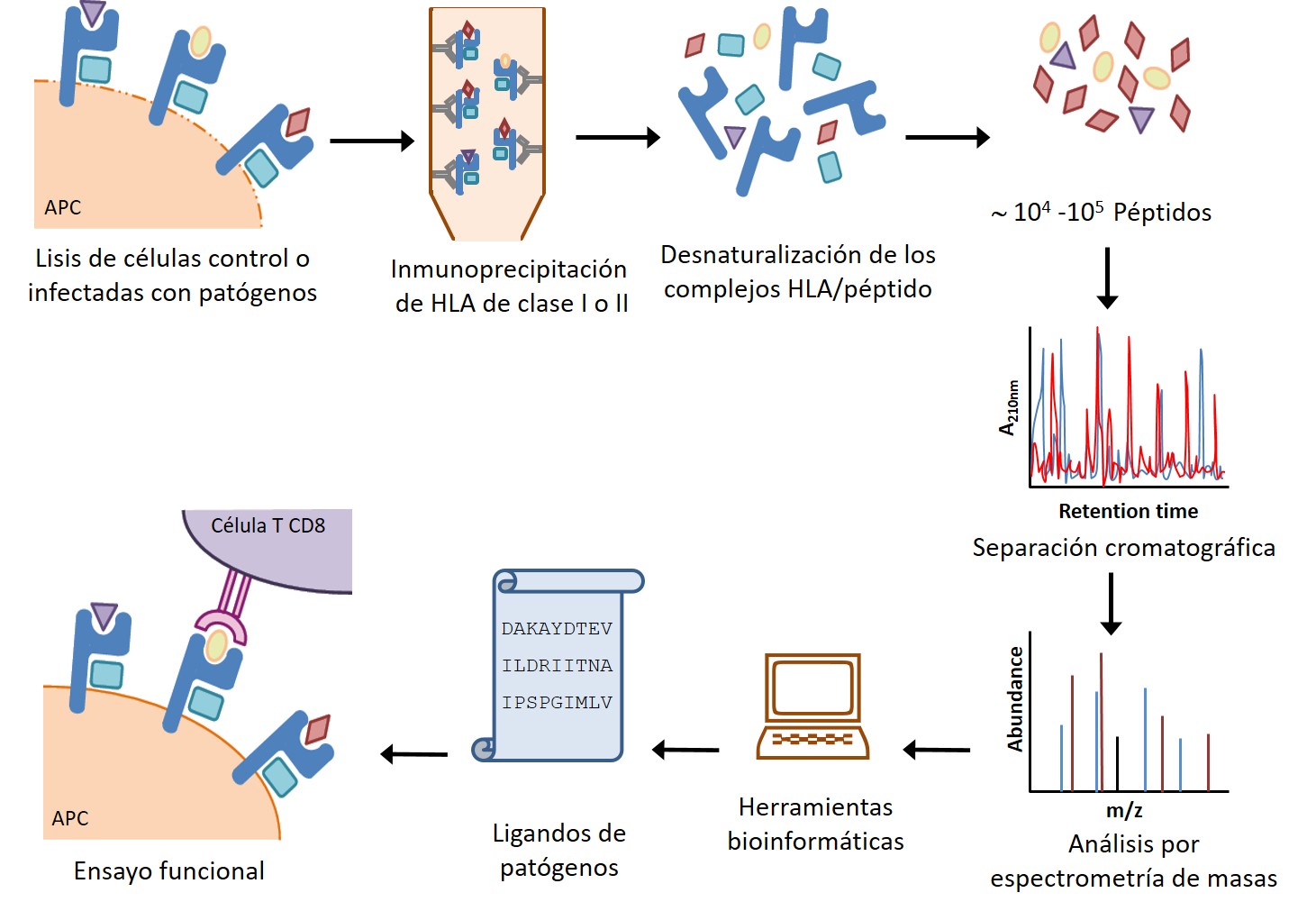
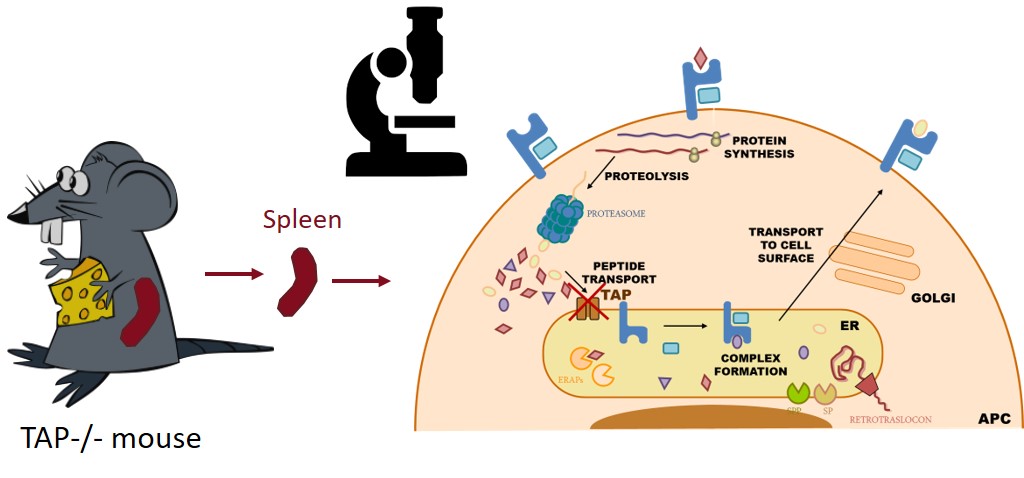
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

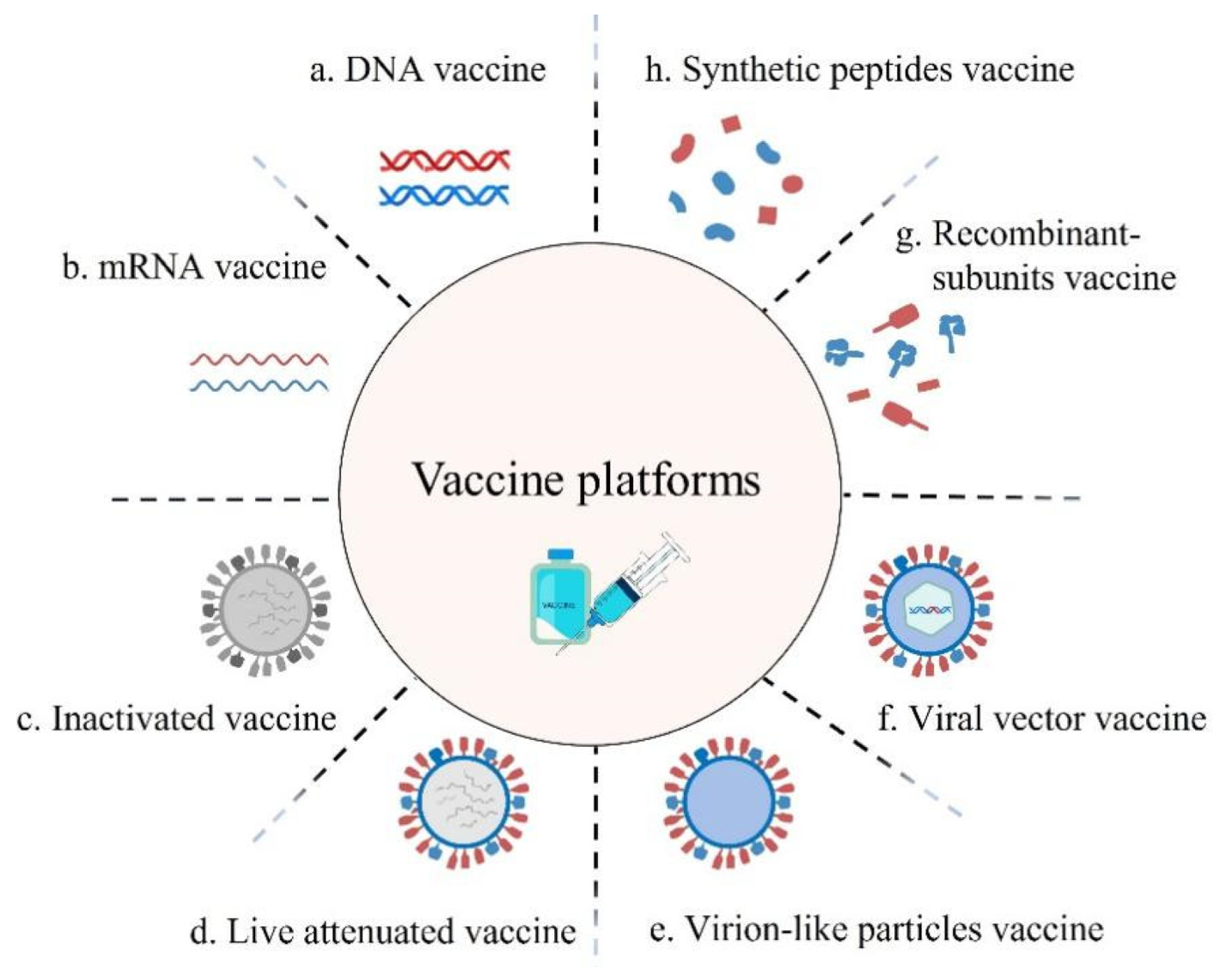
* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
Inmunología Celular
null
The Immunobiology group has been working for years on the following lines of research:
1) The mechanisms of haematopoietic cell generation throughout ontogeny and the influence that the first haematopoietic cells exert on the innate and adaptive immune system present in the adults. We have identified and characterised a new population of B lymphocytes called B1-Rel (B220lo), which produce high levels of natural IgG/IgA antibodies. We sought to understand their role in the immune response in animal models of infection, analysing their impact on immune cell populations and on the production of soluble mediators (cytokines and immunoglobulins). In this regard, we have evaluated the generation of embryonic megakaryocytes (and their differentiation niches), their functionality and that of platelets, and their influence on haematopoietic development. For lymphoid populations, we have carried out extensive characterisation by flow cytometry and single cell RNA sequencing (scRNAseq) methodology. To carry out these cellomic studies, we have designed complex panels for use in multiparametric phenotypic analysis, and single cell cytometry and RNAseq omics technologies on purified cell populations.
In parallel, we are interested in understanding local immune responses in respiratory infections at times of particular susceptibility due to the fragility of the immune system (childhood and old age), both in mouse animal models, which allow their manipulation, and in humans.
2) Mouse models studied during neonatal life, in which we evaluated the effect of antibiotic (AB) treatment and addressed the role of TLR receptors in innate, pseudo-innate and adaptive immune cell populations. In these models, we observed that AB administration was able to modulate B-lymphoid populations, as well as their ability to secrete proinflammatory cytokines in culture and their differentiation into plasma cells, with differentiated immunoglobulin repertoires. Furthermore. These effects were mediated through the Toll-like receptor-2 (TLR2).
3) Mouse models with accelerated senescence (SAMP8) and senescent animals (over 20 months of age) to map lymphoid populations and soluble mediators of the immune response (immunoglobulins and cytokines). In these models, the B lymphoid populations (B1Rel and marginal zone B lymphocytes) are observed to be altered, accompanied by an increase in IgG1 with great restriction of their VDJ repertoires.
4) Role of the B1Rel population in animal models of local or systemic infection. We analysed the response to Streptoccoccus pneumoniae (SPN) locally in the lung and systemically in the spleen, as well as the role of TLR4 in these responses.
5) In humans, we are studying immune responses in children with respiratory syncytial virus (RSV) viral primo-infection. In this case we studied the immune response that occurs locally in the nasal mucosa (by analysis of nasal washings, NW) in a cohort of infected children versus healthy controls, stratified by age. We found that lymphomyeloid cells accumulate in these nasal washings in patients with diverse lymphocyte populations, as well as cytokines and immunoglobulins.
6) Analysis and characterisation of extracellular vesicles produced during respiratory infection both in lung supernatants from models of SPN infection and in LN in the case of children with RSV infection.
7) In parallel, we carry out studies of the genetic rearrangements of immunoglobulins and their use in the generation of chimeric receptors for possible use in immunotherapy.
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “Enfoques inmunoinformaticos e inmunoproteomicos para identificar epitopos bacterianos implicados en la REA: diagnostico temprano y diseño de farmacos” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia, Innovación y Universidades. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Investigador principal. Año: 2024-2026. Presupuesto Concedido: 225.000 euros. Proyecto PID2023-148729OB-100 financiado por MICIU/AEI/10.13039/501100011033 y por FEDER, UE.
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" inanciado por el Plan Nacional de I+D+i del Ministerio de Ciencia, Innovación y Universidades. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Proyecto PID2021-125757OB-100 financiado por MICIU/AEI/10.13039/501100011033 y por FEDER, UE.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
-Project “Induction, differentiation and modulation of resident B lymphocytes in the lung in response to pneumococcus (NEUBLUNG)”. Ministry of Science and Innovation, PID2022-141754OB-I00 Call 2022 "Knowledge Generation Projects". 09/01/2023-08/31/2026. Financed by MICIU/AEI /10.13039/501100011033 and by ERDF, EU. PI: Belén by Andrés Muguruza. CoPI: María Luisa Gaspar Alonso-Vega.
-Project." Immune response of the nasal mucosa in childhood bronchiolitis” Instituto de Salud Carlos III-AESI. AESI-PI22CIII/00030 PI: Belén by Andrés Muguruza. CoPI Maria Luisa Gaspar Alonso-Vega. 01/01/2023-12/31/2025..
-Project. BenBedPhar. CA20121, European Union. Antonio Cuadrado. (CNM-ISCIII).10/19/2021-10/18/2025.
-Spanish Association Against Cancer Project “Novel comprehensive immunotherapy to specifically target the malignant clone in Sézary syndrome, an ultra-rare cancer of mature T lymphocytes”, number PROYE20084REGU. PI: José Ramón Regueiro, PI group Maria Luisa Gaspar. 01/01/2021-12/31/2023.
Project “The pulmonary immune system in homeostasis and infection: characterization and function of immature and pseudoinnate lymphoid populations.” MINECO-RETOS RTI2018-099114-B-100. PI: Maria Luisa Gaspar, CoPI: Belén de Andrés 01/01/2019-12/31/2022. Financed by MICIU/AEI /10.13039/501100011033/ and by FEDER A way of making Europe.
-Project “New B lymphoid populations: B1-rel pseudoinnate cells, homeostatic maintenance and their response under infection conditions.” MINECO-RETOS SAF2015-70880-R. PI: Maria Luisa Gaspar. 01/01/2016-12/31/2019.
-Project “Role of CD19+CD45R lymphocytes- in perinatal immune responses. Implications related to respiratory diseases in neonates. AESI PI14CIII/00049; PI Belén de Andrés. 2015-2018.
-Project “Study of the pseudo-innate population of CD19+CD45R- B lymphocytes in TLR-dependent infection models”. AESI PI11/01733FIS. PI Belén de Andrés. 2012-2015.
-Project." Cellular interactions in the establishment of B lymphoid differentiation niches: role of megakaryocytes and their implications in pathology. MINECO; SAF2012-33916. Maria Luisa Gaspar. 01/01/2013-12/31/2015.
-ISCIII Platforms Project to support R&D&I in Biomedicine and Health Sciences. PT23CIII/00006. 2023. Participating researcher: Isabel Cortegano.
-Research contracts between the Carlos III Health Institute and Inmunotek S.L. for the development of the Bactek-mv130 and Uromune-MV140 study in protection against S. pneumoniae infections. Immunotek. IP: Belen de Andrés 2019-2021.
-Research contract between the Carlos III Health Institute and Inmunotek S.L. “MV130 as a vaccine model based on trained immunity against respiratory infections due to pneumococcus and respiratory syncytial virus”, CAM Call. Industrial Doctorates. IND2023/BMD-27071. PI: Belén by Andrés Muguruza. 12/01/2023-11/30/2026.
- Titulo: “Inmunidad entrenada en trasplante de órganos”.
Entidad financiadora. Ministerio de Ciencia, Innovación y Universidades
Referencia: Proyecto PID2019-110015RB-I00 financiado por MICIU/AEI/10.13039/501100011033
IP: Jordi Cano Ochando
Fechas de ejecución: 01/06/2020-31/05/2024
Presupuesto: 205.700 €
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Outbreak of invasive meningococcal disease caused by a meningococcus serogroup B expressing a rare porA genosubtype (19-54, 15), Spain, March to April 2024.
Abad R, Navarro C, García-Amil C, Montes M, Castañeda-García A, Cuadros JA, Galar A, Martin F, Mena E, Pérez de Madrid S, Román C, Soler M, Vázquez JA. Euro Surveill. 2025 Nov;30(44):2500222
PUBMED DOITrends in invasive bacterial diseases during the first 2 years of the COVID-19 pandemic: analyses of prospective surveillance data from 30 countries and territories in the IRIS Consortium
Shaw D, Abad R, Amin-Chowdhury Z, Bautista A, Bennett D, Broughton K, Cao B, Casanova C, Choi EH, Chu YW, Claus H, Coelho J, Corcoran M, Cottrell S, Cunney R, Cuypers L, Dalby T, Davies H, de Gouveia L, Deghmane AE, Demczuk W, Desmet S, Domenech M, Drew R, du Plessis M, Duarte C, Erlendsdóttir H, Fry NK, Fuursted K, Hale T, Henares D, Henriques-Normark B, Hilty M, Hoffmann S, Humphreys H, Ip M, Jacobsson S, Johnson C, Johnston J, Jolley KA, Kawabata A, Kozakova J, Kristinsson KG, Krizova P, Kuch A, Ladhani S, Lâm TT, León ME, Lindholm L, Litt D, Maiden MCJ, Martin I, Martiny D, Mattheus W, McCarthy ND, Meehan M, Meiring S, Mölling P, Morfeldt E, Morgan J, Mulhall R, Muñoz-Almagro C, Murdoch D, Murphy J, Musilek M, Mzabi A, Novakova L, Oftadeh S, Perez-Argüello A, Pérez-Vázquez M, Perrin M, Perry M, Prevost B, Roberts M, Rokney A, Ron M, Sanabria OM, Scott KJ, Sheppard C, Siira L, Sintchenko V, Skoczyńska A, Sloan M, Slotved HC, Smith AJ, Steens A, Taha MK, Toropainen M, Tzanakaki G, Vainio A, van der Linden MPG, van Sorge NM, Varon E, Vohrnova S, von Gottberg A, Yuste J, Zanella R, Zhou F, Brueggemann AB. Lancet Digit Health. 2023 Sep;5(9):e582-e593.
PUBMED DOIEffectiveness of a Meningococcal Group B Vaccine (4CMenB) in Children
Castilla J, García Cenoz M, Abad R, Sánchez-Cambronero L, Lorusso N, Izquierdo C, Cañellas Llabrés S, Roig J, Malvar A, González Carril F, Boone ALD, Pérez Martín J, Rodríguez Recio MJ, Galmés A, Caballero A, García Rojas A, Juanas F, Nieto M, Viloria Raymundo LJ, Martínez Ochoa E, Rivas AI, Castrillejo D, Moreno Pérez D, Martínez A, Borràs E, Sánchez Gómez A, Pastor E, Nartallo V, Arteagoitia JM, Álvarez-Fernández B, García Pina R, Fernández Arribas S, Vanrell J, García Hernández S, Mendoza RM, Méndez M, López-Tercero MM, Fernández-Rodríguez Á, Blanco Á, Carrillo de Albornoz FJ, Ruiz Olivares J, Ruiz-Montero R, Limia A, Navarro-Alonso JA, Vázquez JA, Barricarte A. N Engl J Med. 2023 Feb 2;388(5):427-438
PUBMED DOIPertactin-Deficient Bordetella pertussis with Unusual Mechanism of Pertactin Disruption, Spain, 1986-2018
14. Mir-Cros A, Moreno-Mingorance A, Martín-Gómez MT, Abad R, Bloise I, Campins M, González-Praetorius A, Gutiérrez MN, Martín-González H, Muñoz-Almagro C, Orellana MÁ, de Pablos M, Roca-Grande J, Rodrigo C, Rodríguez ME, Uriona S, Vidal MJ, Pumarola T, Larrosa MN, González-López JJ. Emerg Infect Dis. 2022 May;28(5):967-976
PUBMED DOIHigh susceptibility to zoliflodacin and conserved target (GyrB) for zoliflodacin among 1209 consecutive clinical Neisseria gonorrhoeae isolates from 25 European countries, 2018.
Unemo M, Ahlstrand J, Sánchez-Busó L, Day M, Aanensen D, Golparian D, Jacobsson S, Cole MJ, Torreblanca RA, Ásmundsdóttir LR, Balla E, De Baetselier I, Bercot B, Carannante A, Caugant D, Borrego MJ, Buder S, Cassar R, Cole M, Dam A, Eder C, Hoffmann S, Hunjak B, Jeverica S, Kirjavainen V, Maikanti-Charalambous P, Miriagou V, Mlynarczyk-Bonikowska B, Pakarna G, Patterson L, Pavlik P, Perrin M, Shepherd J, Stefanelli P, Unemo M, Jelena V, Zákoucká H. J Antimicrob Chemother. 2021 Feb 10:dkab024
PUBMED DOIFirst Insight into the Genome Sequences of Two Linezolid-Resistant Nocardia farcinica Strains Isolated from Patients with Cystic Fibrosis
2: Valdezate S, Monzón S, Garrido N, Zaballos A, Medina-Pascual MJ, Azcona-Gutiérrez JM, Vilar B, Cuesta I. First Insight into the Genome Sequences of Two Linezolid-Resistant Nocardia farcinica Strains Isolated from Patients with Cystic Fibrosis. Genome Announc. 2017 Nov 16;5(46).
PUBMED DOIApoptosis, Toll-like, RIG-I-like and NOD-like Receptors Are Pathways Jointly Induced by Diverse Respiratory Bacterial and Viral Pathogens.
3: Martínez I, Oliveros JC, Cuesta I, de la Barrera J, Ausina V, Casals C, de Lorenzo A, García E, García-Fojeda B, Garmendia J, González-Nicolau M, Lacoma A, Menéndez M, Moranta D, Nieto A, Ortín J, Pérez-González A, Prat C, Ramos-Sevillano E, Regueiro V, Rodriguez-Frandsen A, Solís D, Yuste J, Bengoechea JA, Melero JA. Apoptosis, Toll-like, RIG-I-like and NOD-like Receptors Are Pathways Jointly Induced by Diverse Respiratory Bacterial and Viral Pathogens. Front Microbiol. 2017 Mar 1;8:276
PUBMED DOIMolecular identification, antifungal resistance and virulence of Cryptococcus neoformans and Cryptococcus deneoformans isolated in Seville, Spain
Gago S, Serrano C, Alastruey-Izquierdo A, Cuesta I, Martín-Mazuelos E, Aller AI, Gómez-López A, Mellado E. Molecular identification, antifungal resistance and virulence of Cryptococcus neoformans and Cryptococcus deneoformans isolated in Seville, Spain. Mycoses. 2017 Jan;60(1):40-50
PUBMED DOIHigh-Quality Draft Genome Sequence of Babesia divergens, the Etiological Agent of Cattle and Human Babesiosis
7: Cuesta I, González LM, Estrada K, Grande R, Zaballos A, Lobo CA, Barrera J, Sanchez-Flores A, Montero E. High-Quality Draft Genome Sequence of Babesia divergens, the Etiological Agent of Cattle and Human Babesiosis. Genome Announc. 2014 Nov 13;2(6).
PUBMED DOISerum galactomannan-based early detection of invasive aspergillosis in hematology patients receiving effective antimold prophylaxis
8: Duarte RF, Sánchez-Ortega I, Cuesta I, Arnan M, Patiño B, Fernández de Sevilla A, Gudiol C, Ayats J, Cuenca-Estrella M. Serum galactomannan-based early detection of invasive aspergillosis in hematology patients receiving effective antimold prophylaxis. Clin Infect Dis. 2014 Dec 15;59(12):1696-702.
PUBMED DOIAnalysis of the protein domain and domain architecture content in fungi and its application in the search of new antifungal targets.
9: Barrera A, Alastruey-Izquierdo A, Martín MJ, Cuesta I, Vizcaíno JA. Analysis of the protein domain and domain architecture content in fungi and its application in the search of new antifungal targets. PLoS Comput Biol. 2014 Jul 17;10(7):e1003733.
PUBMED DOICryptococcus neoformans can form titan-like cells in vitro in response to multiple signals
2. Trevijano-Contador N, de Oliveira HC, García-Rodas R, Rossi SA, Llorente I, Zaballos Á, Janbon G, Ariño J, Zaragoza Ó. Cryptococcus neoformans can form titan-like cells in vitro in response to multiple signals. PLoS Pathog. 2018 May 18;14(5):e1007007.
PUBMED DOIReclassification of the Candida haemulonii complex as Candida haemulonii (C. haemulonii group I), C. duobushaemulonii sp. nov. (C. haemulonii group II), and C. haemulonii var. vulnera var. nov.: three multiresistant human pathogenic yeasts
4. Cendejas-Bueno E, Kolecka A, Alastruey-Izquierdo A, Theelen B, Groenewald M, Kostrzewa M, Cuenca-Estrella M, Gómez-López A, Boekhout T. Reclassification of the Candida haemulonii complex as Candida haemulonii (C. haemulonii group I), C. duobushaemulonii sp. nov. (C. haemulonii group II), and C. haemulonii var. vulnera var. nov.: three multiresistant human pathogenic yeasts. J Clin Microbiol.
PUBMED DOIMolecular Identification and Susceptibility Testing of Molds Isolated in a Prospective Surveillance of Triazole Resistance in Spain (FILPOP2 Study).
5. Alastruey-Izquierdo A, Alcazar-Fuoli L, Rivero-Menéndez O, Ayats J, Castro C, García-Rodríguez J, Goterris-Bonet L, Ibáñez-Martínez E, Linares-Sicilia MJ, Martin-Gomez MT, Martín-Mazuelos E, Pelaez T, Peman J, Rezusta A, Rojo S, Tejero R, Anza DV, Viñuelas J, Zapico MS, Cuenca-Estrella M; the FILPOP2 Project from GEMICOMED (SEIMC) and REIPI. Molecular Identification and Susceptibility Testing of Molds Isolated in a Prospective Surveillance of Triazole Resistance in Spain (FILPOP2 Study). Antimicrob Agents Chemother. 2018 Aug 27;62(9).
PUBMED DOIEvaluation of Bronchoalveolar Lavage Fluid Cytokines as Biomarkers for Invasive Pulmonary Aspergillosis in At-Risk Patients
6. Gonçalves SM, Lagrou K, Rodrigues CS, Campos CF, Bernal-Martínez L, Rodrigues F, Silvestre R, Alcazar-Fuoli L, Maertens JA, Cunha C, Carvalho A. Evaluation of Bronchoalveolar Lavage Fluid Cytokines as Biomarkers for Invasive Pulmonary Aspergillosis in At-Risk Patients. Front Microbiol. 2017 Nov 29;8:2362.
PUBMED DOIPolymorphisms in Host Immunity-Modulating Genes and Risk of Invasive Aspergillosis: Results from the AspBIOmics Consortium
7. Lupiañez CB, Canet LM, Carvalho A, Alcazar-Fuoli L, Springer J, Lackner M, Segura-Catena J, Comino A, Olmedo C, Ríos R, Fernández-Montoya A, Cuenca-Estrella M, Solano C, López-Nevot MÁ, Cunha C, Oliveira-Coelho A, Villaescusa T, Fianchi L, Aguado JM, Pagano L, López-Fernández E, Potenza L, Luppi M, Lass-Flörl C, Loeffler J, Einsele H, Vazquez L; PCRAGA Study Group, Jurado M, Sainz J. Polymorphisms in Host Immunity-Modulating Genes and Risk of Invasive Aspergillosis: Results from the AspBIOmics Consortium. Infect Immun. 2015 Dec 14;84(3):643-57.
PUBMED DOICell Wall Changes in Amphotericin B-Resistant Strains from Candida tropicalis and Relationship with the Immune Responses Elicited by the Host.
9. Mesa-Arango AC, Rueda C, Román E, Quintin J, Terrón MC, Luque D, Netea MG, Pla J and Zaragoza O. Cell Wall Changes in Amphotericin B-Resistant Strains from Candida tropicalis and Relationship with the Immune Responses Elicited by the Host. Antimicrob. Agents Chemother. 2016. 60(4):2326-35.
PUBMED DOIThe role of respiratory viruses in children with humoral immunodeficiency on immunoglobulin replacement therapy
Benavides-Nieto M, Méndez-Echevarría A, Del Rosal T, García-García ML, Casas I, Pozo F, de la Serna O, Lopez-Granados E, Rodriguez-Pena R, Calvo C. The role of respiratory viruses in children with humoral immunodeficiency on immunoglobulin replacement therapy. Pediatr Pulmonol. 2019 Feb;54(2):194-199. Indice Impacto: 3,157. Revista en Q1.
PUBMED DOISeasonality and geographical spread of respiratory syncytial virus epidemics in 15 European countries, 2010 to 2016.
Broberg EK, Waris M, Johansen K, Snacken R, Penttinen P; European Influenza Surveillance Network. Seasonality and geographical spread of respiratory syncytial virus epidemics in 15 European countries, 2010 to 2016. Euro Surveill. 2018 Feb;23(5). Indice Impacto: 5,983. Revista en Decil 1
PUBMED DOIHuman Metapneumovirus infections in hospitalized children and comparison with other respiratory viruses in 2005-2014 prospective study.
García-García ML, Calvo C, Rey C, Díaz B, Molinero MD, Pozo F, Casas I. Human Metapneumovirus infections in hospitalized children and comparison with other respiratory viruses in 2005-2014 prospective study. PLoS One. 2017 Mar 16;12(3):e0173504. doi: 10.1371/journal.pone.0173504. eCollection 2017. Indice Impacto: 2,766. Revista en Q1.
PUBMED DOIRespiratory Infections by Enterovirus D68 in Outpatients and Inpatients Spanish Children
Calvo C, Cuevas MT, Pozo F, García-García ML, Molinero M, Calderón A, Gonzalez-Esguevillas M, Pérez-Sautu U, Casas I. Respiratory Infections by Enterovirus D68 in Outpatients and Inpatients Spanish Children. Pediatr Infect Dis J. 2016 Jan;35(1):45-9.
PUBMED DOIClinical and Virologic Characteristics of Early and Moderate Preterm Infants Readmitted with Viral Respiratory Infections.
García-Garcia ML, González-Carrasco E, Quevedo S, Muñoz C, Sánchez-Escudero V, Pozo F, Casas I, Calvo C. Clinical and Virologic Characteristics of Early and Moderate Preterm Infants Readmitted with Viral Respiratory Infections. Pediatr Infect Dis J. 2015 Jul;34(7):693-9. Indice Impacto: 2,587. Revista en Q1
PUBMED DOIEight Year Prospective Study of Adenoviruses Infections in Hospitalized Children. Comparison with Other Respiratory Viruses.
Calvo C, García-García ML, Sanchez-Dehesa R, Román C, Tabares A, Pozo F, Casas I. Eight Year Prospective Study of Adenoviruses Infections in Hospitalized Children. Comparison with Other Respiratory Viruses. PLoS One. 2015 Jul 6;10(7):e0132162. eCollection 2015. Indice Impacto: 3,057. Revista en Q1
PUBMED DOIInfluenza vaccine effectiveness in Spain 2013/14: subtype-specific early estimates using the cycEVA study
Jiménez-Jorge S, Pozo F, de Mateo S, Delgado-Sanz C, Casas I, García-Cenoz M, Castilla J, Sancho R, Etxebarriarteun-Aranzabal L, Quinones C, Martínez E, Vega T, Garcia A, Giménez J, Vanrell JM, Castrillejo D, Larrauri A, on behalf of the Spanish Influenza Sentinel Surveillance System (SISS). Influenza vaccine effectiveness in Spain 2013/14: subtype-specific early estimates using the cycEVA study. Euro Surveill. 2014 Mar 6;19(9). Indice Impacto: 5,722. Revista en Q1.
PUBMED DOIY155H amino acid substitution in influenza A(H1N1)pdm09 viruses does not confer a phenotype of reduced susceptibility to neuraminidase inhibitors
Perez-Sautu U, Pozo F, Cuesta I, Monzon S, Calderon A, Gonzalez M, Molinero M, Lopez-Miragaya I, Rey S, Cañizares A, Rodriguez G, Gonzalez-Velasco C, Lackenby A, Casas I. Y155H amino acid substitution in influenza A(H1N1)pdm09 viruses does not confer a phenotype of reduced susceptibility to neuraminidase inhibitors. Euro Surveill. 2014 Jul 10;19(27):14-20. Indice Impacto: 5,722. Revista en Q1
PUBMED DOICharacterization In Vitro and In Vivo of a Pandemic H1N1 Influenza Virus from a Fatal Case.
Rodriguez A, Falcon A, Cuevas MT, Pozo F, Guerra S, García-Barreno B, Martinez-Orellana P, Pérez-Breña P, Montoya M, Melero JA, Pizarro M, Ortin J, Casas I, Nieto A. Characterization In Vitro and In Vivo of a Pandemic H1N1 Influenza Virus from a Fatal Case. PLoS One. 2013;8(1):e53515. doi: 10.1371/journal.pone.0053515. Epub 2013 Jan 10. Indice Impacto: 3,534. Revista en Q1
PUBMED DOIMycobacterium tuberculosis genotypes and predominant clones among the multidrug-resistant isolates in Spain 1998-2006
3. Samper S, Gavin P, Millan-Lou MI, Iglesias M.J. Jimenez MS. Spanish Working Group on MDR-TB, Covin D, Rastogi N. Mycobacterium tuberculosis genotypes and predominant clones among the multidrug-resistant isolates in Spain 1998-2006. Infec Genet Evol. 2017. Aug 5;55:117.
PUBMED DOIAntitubercular drugs for an old target: GSK693 as a promising inhA direct inhibitor.
5. Martinez-Hoyos M, Perez-Herran E, Gulten G, Encinas L, Alvarez-Gomez D, Alvarez E, Ferrer Bazaga S, Garcia-Perez A, Ortega F, Angulo-Bartures I, Rullas-Trincado J, Blanco Ruano D, Torres P, Castañeda P, Huss S, Fernandez R, Gonzalez del Valle S, Ballel L, Barros D, Modha S, Dhar N, Signorino-Gelo F, McKinney JD, Garcia-Bustos JF, Lavandera JL, Sacchettini JC, Jimenez MS, Martin-Casabona N, Castro-PIchel J, Mendoza-Losana A. Antitubercular drugs for an old target: GSK693 as a promising inhA direct inhibitor. EBioMedicine. 2016; 8:291-301
PUBMED DOIPediatric drug-resistant tuberculosis in Madrid family matters
7. Santiago B, Baquero-Artiago F, Mejias A, Blázquez D, Jimenez MS, Mellado-Peña MJ, EREMITA Study group. Pediatric drug-resistant tuberculosis in Madrid: family matters. The Pediatric Infectious Disease Journal. 2014; 33:345-350.
PUBMED DOIMycobacterium kumamotonense, another Member of the Mycobacterium terrae Complex Unusually Carrying Two Copies of the Ribosomal RNA Operon
8. Menéndez MC, Jiménez MS, Yubero J, García MJ. Mycobacterium kumamotonense, another Member of the Mycobacterium terrae Complex Unusually Carrying Two Copies of the Ribosomal RNA Operon. Mycobac Dis; 2014; 4:176.
DOI