Viral Infection and Immunity
Líneas de investigación
Arbovirus y Enfermedades víricas importadas
El laboratorio de Arbovirus y Enfermedades Víricas Importadas (AEVI) del CNM desarrolla su trabajo dentro de la línea de investigación “Virus emergentes transmitidos por vector y/o reservorio, de importancia en salud pública”, que se sustenta en las áreas de epidemiología molecular, desarrollo metodológico, detección en vectores y reservorios y, otros aspectos relacionados con estas zoonosis con una aplicación clara hacia la investigación, prevención, preparación, control y respuesta a las amenazas o brotes causados por estos virus.
Arbovirus como Dengue, Chikungunya o Zika son virus endémicos en todo el cordón tropical/sub-tropical del planeta en continua expansión a latitudes más lejanas debido al calentamiento global y a la dispersión y colonización de nuevos hábitats llevada a cabo por sus vectores artrópodos y son transportados a otras zonas del planeta a través de pacientes virémicos por lo que si, como ocurre en España, se cuenta con vectores transmisores establecidos, se puede propiciar el establecimiento de circulación autóctona. Además de estos virus exóticos, en España circulan endémicamente los arbovirus Toscana, West Nile y el virus de la Fiebre hemorrágica de Crimea-Congo, entre otros.
La OMS elaboró un listado en 2019 con las 10 amenazas para la Salud Global que consideraron más importantes, entre las que se encuentran los virus Dengue, Ébola y Zika. El principal temor es que la falta de preparación cause una epidemia. Además, algunos de estos virus como Dengue y Chikungunya son considerados también “Enfermedades Tropicales Desatendidas” que ponen en peligro la salud de muchas personas en países empobrecidos sin que se estudien con los recursos necesarios.
La importancia para la salud pública de estos patógenos, y la necesidad de prepararse frente a ellos, se refleja también en la lista de actividades prioritarias de investigación y desarrollo de la OMS que actualmente incluye, entre otros, el Ébola, el virus de la Fiebre Hemorrágica de Crimea Congo, el virus de Zika y la enfermedad por el virus de Nipah, debido a la amenaza que suponen para la Salud Pública por su potencial epidémico o porque no hay medidas de control suficientes. Además del peligro real que representan en zonas endémicas, algunos de los virus mencionados (Ébola, Zika, West Nile, Crimea-Congo y Dengue) han supuesto, y continúan siendo, una amenaza para nuestro país habiendo producido casos esporádicos o brotes localizados de infección autóctona. El riesgo para España de las enfermedades transmitidas por vectores está aumentando de manera muy clara como se ha podido observar en los últimos años, y la previsión es que siga aumentando.
Todos estos virus son virus zoonóticos emergentes y nuestro grupo de investigación lleva décadas trabajando en diferentes aspectos en relación con estos patógenos. El riesgo de emergencia y expansión de estos virus se basa de sus ciclos complejos de transmisión, por lo que nuestros estudios se basan tanto en el ser humano, como en los reservorios y los vectores que los transmiten. De esta base, parten transversalmente las líneas de actuación que van enfocadas a estudios de epidemiología molecular, desarrollo metodológico, detección de virus en vectores y hospedadores, caracterización de los mismos y estudios de competencia vectorial, con una aplicación dirigida hacia la investigación, prevención y respuesta a las amenazas o brotes causados por estos virus. El trabajo que desarrollamos se articula en torno a 3 objetivos principales:
Objetivo 1. Búsqueda y caracterización de virus emergentes en vectores y/o reservorios. Se lleva a cabo mediante herramientas moleculares incluyendo las nuevas estrategias de NGS, de virus emergentes en vectores y reservorios. De los virus detectados se realiza una caracterización molecular y serológica, llevando a cabo estudios de epidemiología molecular y de relaciones genéticas y antigénicas con virus relacionados.
Objetivo 2. Desarrollo metodológico para detección, identificación y caracterización de virus emergentes. Los métodos desarrollados pueden transferirse al SNS, explotarse comercialmente y/o utilizarse en la Cartera de Servicios del CNM. Estos desarrollos moleculares, y/o serológicos, refuerzan al CNM en su papel como Laboratorio Nacional de Referencia de Zoonosis, con un aporte de herramientas útiles y necesarias para la detección y caracterización de estos agentes. De igual forma, el desarrollo de herramientas tipo flujo lateral, las denominadas “Point Of Care” es una de las necesidades que pretendemos dar solución.
Objetivo 3. Eco-epidemiología de viriasis emergentes. Debido a los complejos ciclos biológicos de los arbovirus, el estudio de las especies de vectores implicados en nuestro país, así como el origen y evolución de los agentes circulantes, es crucial a la hora de entenderlos y responder a las amenazas que generan. Para ello estudiamos la presencia de estos virus tanto en muestras humanas como de vectores y posibles hospedadores, lo que nos permite, con un enfoque de “Una Salud”, entender los mecanismos que controlan su circulación y que puedan estar implicados en su patogenicidad.
Babesiosis
null
Bacterial Genetics
Our group has been studying for more than 30 years the mechanisms of antibiotic resistance in Streptococcus pneumoniae (Spn). Our objectives are to understand the molecular basis of antimicrobial action, to search for new targets of action and new compounds. Seconeolitsine (SCN) is one of these new compounds targeting topoisomerase I (Topo I). As for the search for new targets, our research has focused in recent years on the factors that organize the topology of the chromosome, allowing optimal compaction (about 1000-fold) to harmonize its replication, chromosome segregation and gene expression. This compaction is mediated both by the level of DNA supercoiling (Sc) and by association with nucleoid-binding proteins (NAPs). The level of Sc depends mainly on the enzymatic activities of their DNA topoisomerases, reaching a homeostatic equilibrium by the opposite activities of the topoisomerases that relax DNA (Topo I and Topo IV), and of gyrase, which introduces negative Sc. Our group has characterized the three Spn topoisomerases and two NAPs: HU and SatR. In addition, the availability of antimicrobials that inhibit each of the Spn topoisomerases has allowed us to analyze their transcriptome under conditions of local or global change of the Sc level and to define gene domains of coordinated transcription and similar functions. Fluoroquinolones, which inhibit Topo IV and gyrase, produce local changes in Sc that induce alterations in 6% of the transcriptome, altering metabolic pathways that originate an increase in reactive oxygen species (ROS) that contribute to lethality, in accordance with the general mechanism of bactericidal antibiotics. On the other hand, the induction of global changes in Sc by novobiocin (NOV, gyrase inhibitor), or by SCN (Topo I inhibitor), has allowed us to define topological domains. Global changes in Sc include the regulation of topoisomerase genes: its decrease activates the transcription of gyrase genes (gyrA, gyrB) and inhibits those of Topo IV (parEC) and Topo I (topA); the increase in Sc regulates the expression of topA. Decreased Sc affects 37% of the genome, with >68% of genes clustered in 15 domains. Increased Sc affects 10% of the genome, with 25% of the genes clustered in 12 domains. The AT content in the genome correlates with the domains, being higher in UP domains than in DOWN domains. The genes in the different domains have common functional characteristics, indicating that they have been subjected to topological selective pressure to determine the location of genes involved in metabolism, virulence and competition.
The current objectives of the group are:
1. Identification of factors that stabilize chromosome topology: NAPs, ncRNAs, intra-chromosomal interactions.
2. Regulation of transcription in response to topological stress: in vivo localization of DNA topoisomerases, RNA polymerase and NAPs.
3. Topo I as a new antimicrobial target and action of SCN.
4. Design of antisense RNAs and use of the CRISPR system as new antibacterial agents.
Biología y Variabilidad del VIH
null
Enfermedades bacterianas transmitidas por agua y alimentos
null
Genomica y Bioinformática
null
Hepatitis
- Diseño de métodos diagnósticos para el estudio de los virus de las hepatitis (VH) A, B, C, D, E: Diseñamos sistemas de PCR para su detección y caracterización.
- Evaluación de métodos diagnósticos de los VH. Colaboramos con empresas para estudios de sensibilidad y especificidad de equipos diagnósticos.
- Estudios de Seroprevalencia de los virus de las hepatitis.
- Epidemiología genómica de genomas completos de VHA, VHB, VHC, VHD y VHE en colaboración con el ECDC. Estudios de trazabilidad del VHE.
- Caracterización molecular de virus de las hepatitis mediante secuenciación masiva: a) VHB: mutantes de escape HBsAg (prevalencia y efectos en la detección del HBsAg). Estudio de mutaciones en epítopos de estimulación inmune y mutaciones asociadas a evolución clínica desfavorable.
- b) VHC: resistencias a los antivirales de acción directa. Análisis molecular de subtipos poco frecuentes.
c) Estudios filogenéticos del VHD.
d) Análisis genómico del VHE.
e) Investigación etiológica de hepatitis no filiadas mediante estudios de metagenómica.
- b) VHC: resistencias a los antivirales de acción directa. Análisis molecular de subtipos poco frecuentes.
Infección Viral e Inmunidad
null
Infecciones relacionadas con la Asistencia Sanitaria
null
Infecciones Víricas e Inmunidad en Enfermos Inmunodeprimidos
Nuestras líneas de investigación se centran en distintas áreas del conocimiento relacionadas con hepatitis virales crónicas (Hepatitis B, C y D), VIH, y SARS-CoV-2:
- Inmunopatogenia de las infecciones virales y su relación con eventos clínicos.
- Impacto en el organismo del control o eliminación de la infección viral.
- Biopsia líquida y ómicas: biomarcadores de enfermedad en infección viral.
- Resistencia a la infección viral y aclaramiento espontáneo.
- Cribado de infección viral y epidemiología molecular de los virus.
- Desarrollo de kits de diagnóstico rápido.
- Respuesta inmune a vacunas.
Infección por CMV en pacientes trasplantados
En los últimos años en nuestro grupo hemos estudiado la cinética de infección por CMV y el desarrollo de la respuesta inmune protectora específica frente a CMV. Como resultados de estos estudios hemos sido capaces de caracterizar la cinética y magnitud de la adquisición de la respuesta inmune frente a CMV y establecer puntos de corte de inmunidad específica que se relacionan con la protección frente a la infección.
El objetivo de esta línea de investigación en los últimos años ha sido definir parámetros relacionados con la respuesta inmune específica frente a CMV y con factores genéticos que puedan estar relacionados con el control de la infección y enfermedad por CMV. El estudio de estas variables de forma conjunta como marcadores de predicción del riesgo de desarrollo de infección/enfermedad y de la evolución de la infección tras el trasplante permitirían establecer un algoritmo para el manejo de los pacientes. Además, permitirían definir niveles mínimos de protección que sirvan de endpoints para el desarrollo de una vacuna. Esta línea de investigación se enmarca dentro del programa de Infecciones en Transplantes de la Red Española de Investigación en Patologías Infecciosas (REIPI), como parte del WP2 denominado Optimización de la prevención de la enfermedad por CMV.
Desarrollo preclínico de vacunas protectoras frente a CMV
La vacuna ideal frente a CMV debería estar compuesta por múltiples antígenos y ser capaz de imitar el efecto producido por la infección natural, y estimular una respuesta inmune específica combinada tanto de células T como de anticuerpos neutralizantes. Sin embargo, a pesar de los esfuerzos realizados y los progresos de los últimos años, los resultados obtenidos en el desarrollo de una vacuna frente a CMV no han mostrado resultados definitivos.
Por tanto, el objetivo de esta línea de investigación es promover aproximaciones innovadoras para el diseño y desarrollo de una vacuna frente a la infección por CMV. Para ello se ha puesto en marcha una aproximación a través de la construcción de un plásmido optimizado para generar una respuesta inmune combinada y amplia específica frente a CMV y la búsqueda de los antígenos candidatos, a través del estudio de la inmunogenicidad in vivo del proteoma completo de CMV.
Desarrollo preclínico de alternativas terapéuticas frente a CMV basadas en la inmunoterapia
La inmunidad mediada por células T constituye una respuesta adaptativa fundamental y representa el mecanismo de defensa más importante frente a la infección viral. Por otra parte, la presencia en suero de anticuerpos neutralizantes se han asociado con tasas más bajas de transmisión del CMV de la madre al feto y en los receptores de trasplante de órgano sólido.
El presente proyecto propone un enfoque novedoso a través de la identificación y caracterización de la respuesta inmune tanto celular como de anticuerpos en pacientes que han sido inmunizados de forma natural y están protegidos frente a la infección por CMV, para abordar el desarrollo preclínico de alternativas terapéuticas basadas en la transferencia adoptiva de células T CD8+ citotóxicas y de anticuerpos monoclonales específicos de CMV con el objetivo de desarrollar una nueva estrategia terapéutica para el tratamiento frente a la infección por este patógeno.
Estudio del desarrollo de inmunidad frente a SARS-CoV-2
Dada la situación producida como consecuencia de la propagación del SARS-CoV-2 urge la realización de estudios serológicos que nos ayuden a determinar el alcance y la duración de la inmunidad adquirida por la población infectada por SARS-CoV-2 que ha superado la enfermedad. En este sentido el estudio de los anticuerpos neutralizantes, que son aquellos que reconocen las proteínas del virus implicadas en el reconocimiento del receptor celular bloqueando su capacidad infectiva, en pacientes recuperados de la infección por SARS-CoV-2 podrían ser clave para explicar el pronóstico de la enfermedad en estos pacientes. Además son necesarios estudios que estudien la cinética de la inmunidad de anticuerpos específicos frente a coronavirus y su relación con la evolución de la enfermedad que nos permitan establecer estrategias de manejo de los pacientes en base a su patrón inmunológico.
También participamos en el desarrollo de un prototipo de vacuna basado en ADN plasmídico que expresa antígenos de SARS-CoV-2 y la caracterización de la respuesta inmune inducida por esta vacuna en un modelo murino de inmunización.
Inmunología Celular
null
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
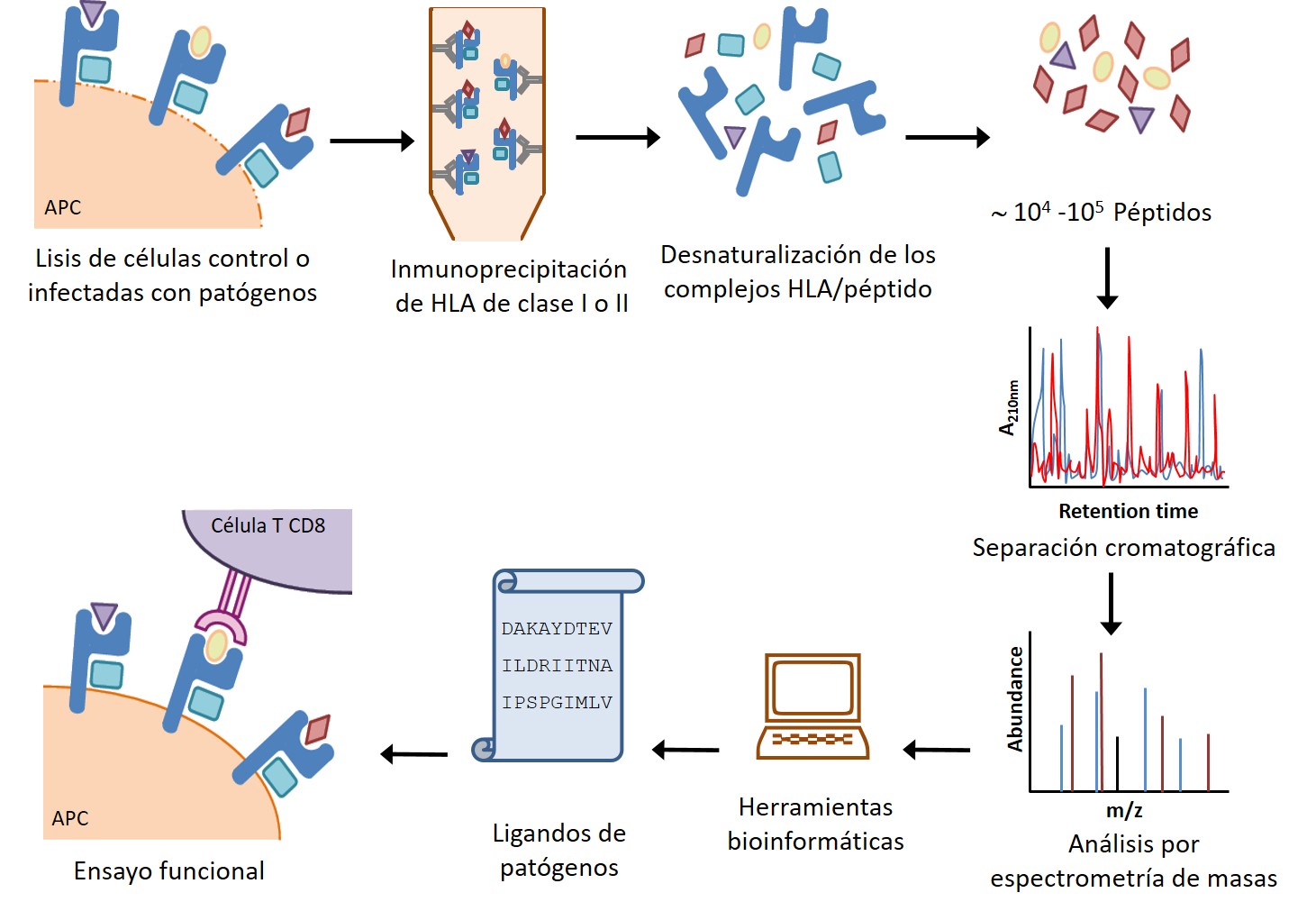
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

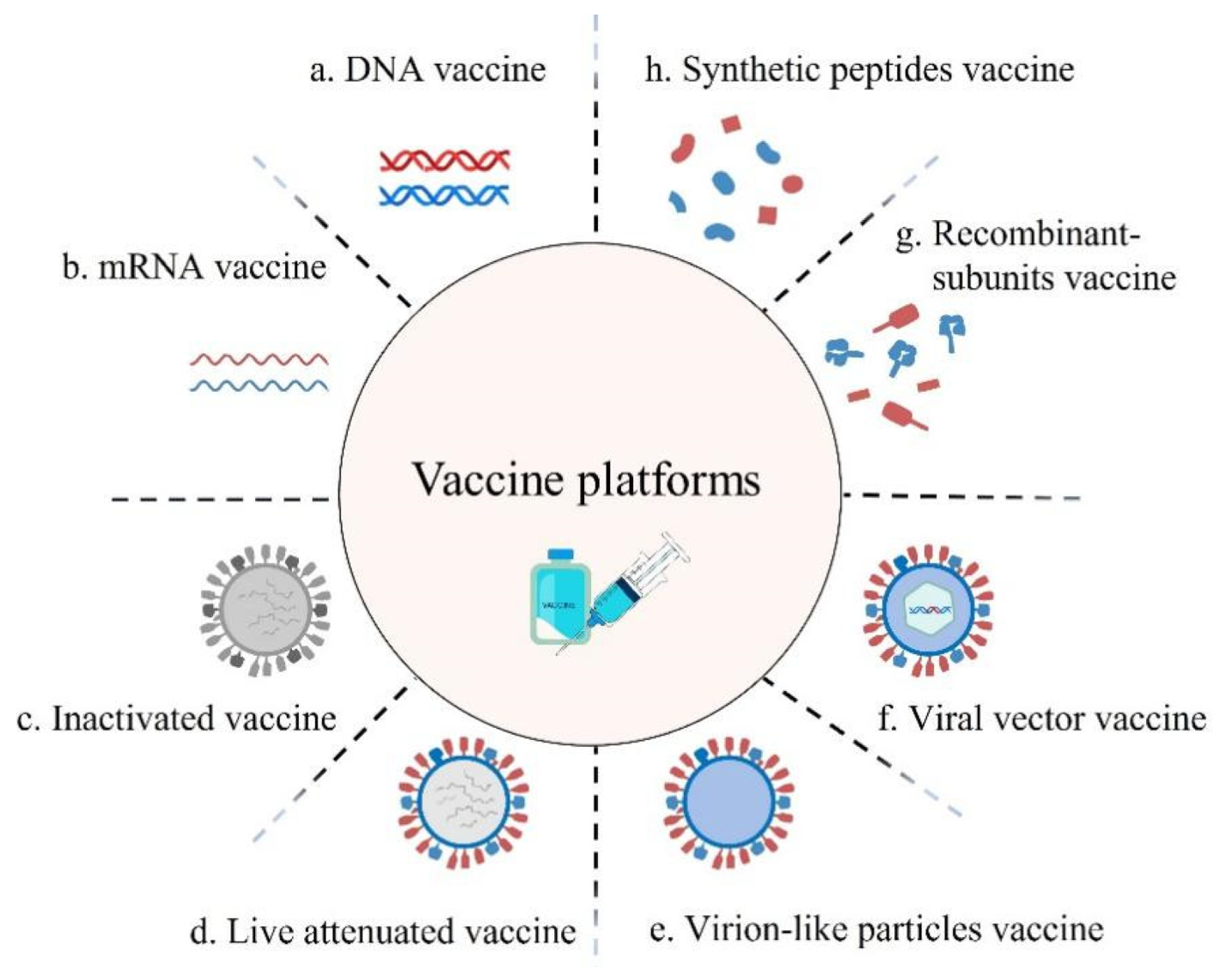
* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
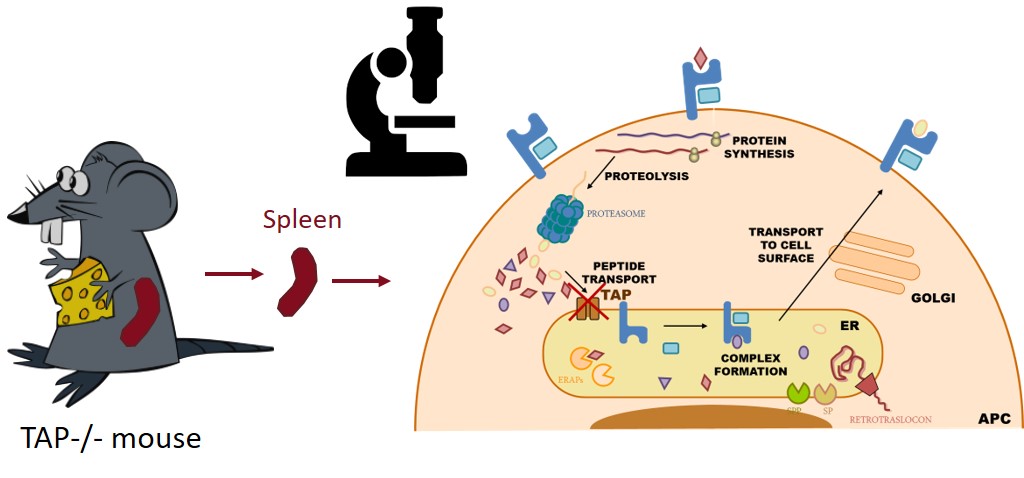
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
Leishmaniasis y Enfermedad de Chagas
null
Malaria y Parasitosis Emergentes
null
Micobacterias
• Estudio taxonómico.
• Estudio de la sensibilidad fenotípica a nuevos fármacos antituberculosos.
• Análisis de las bases moleculares de la resistencia a fármacos antituberculosos.
• Epidemiología molecular de la tuberculosis. • Desarrollo de nuevos métodos de identificación y detección de resistencias en micobacterias.
La tuberculosis (TB) es una enfermedad infecciosa, provocada por un grupo de micobacterias incluidas en el grupo Mycobacterium tuberculosis complex, que puede afectar tanto al hombre como a los animales. Se caracteriza por la formación de tubérculos o nódulos en los tejidos infectados. Su trasmisión es por vía aérea, pero puede afectar a diferentes órganos del cuerpo.
La TB fue declarada emergencia sanitaria mundial por la Asamblea de la Organización Mundial de la Salud (OMS) en el año 1991 y continúa siendo una de las enfermedades infecciosas con mayor incidencia y tasa de mortalidad. Un tercio de la población mundial está infectada, constituyendo el reservorio de la enfermedad. En el año 2019 se estimó que 10 millones de personas contrajeron la enfermedad con 1,2 millones de fallecimientos. En España, el Plan Nacional para la Prevención y Control de la TB fue aprobado en 2019. Recoge los desafíos actuales que giran en torno a la detección precoz de la enfermedad, la realización de estudios de sensibilidad a todas las cepas aisladas, la mejora en el cumplimiento del tratamiento, la realización de estudios de contactos y la aplicación de marcadores epidemiológicos para la detección de brotes.
La aparición de cepas resistentes representa una amenaza para los planes de control y erradicación propuestos por la OMS. La TB multirresistente (MDR) causada por cepas resistentes al menos a Isoniacida y Rifampicina (los fármacos más activos frente a M. tuberculosis complex), requieren para su tratamiento drogas alternativas menos eficaces y peor toleradas, implicando regímenes terapéuticos más prolongados, aumentando la toxicidad y reduciendo las probabilidades de curación. En 2019 se estimó que más de medio millón de personas desarrollaron una TB causada por cepas MDR-TB. La OMS los términos pre-XDR para la TB pre-extemadamente resistente (causada por cepas MDR-TB que además son resistentes a Quinolonas), y XDR (cepas MDR-TB que son resistentes a cualquier Quinolona y al menos a Linezolid o Bedaquilina). Estas cepas producen una TB de muy difícil tratamiento, con escasa probabilidad de curación y terapias muy costosas que agravan el problema de la TB.
Las micobacterias no tuberculosas (MNT) son bacterias ubicuas que se encuentran en el medio ambiente siendo éste su reservorio y la fuente de infección. Taxonómicamente las MNT forman un grupo de especial complejidad por el gran número de especies y por la diversidad biológica entre ellas, que se traduce en una elevada heterogeneidad intraespecífica tanto fenotípica como genotípica, lo que hace que por economía, rentabilidad y organización el Centro Europeo de Control de Enfermedades (ECDC) recomiende la centralización de las labores de identificación y estudios de sensibilidad en laboratorios con un alto grado de especialización y que dispongan de las medidas de bioseguridad adecuadas para el manejo de estas cepas.
El número de casos causado por estas micobacterias, ha sufrido un aumento muy importante en la última década, al utilizar medios de cultivo mejor diseñados para su aislamiento, al uso de técnicas quirúrgicas más agresivas que favorecen la infección por bacterias oportunistas, la utilización de fármacos inmunosupresores, la mayor supervivencia de los pacientes con inmunodeficiencias y, sobre todo a la aparición del VIH.
Micología
null
Microbiología Estructural
null
Neisseria, Listeria y Bordetella
• Invasive Meningococcal Disease.
o Laboratory surveillance based on whole-genome sequencing and its application in Public Health.
o Study and characterization of antimicrobial resistance mechanisms.
o Study and evaluation of conventional (polysaccharide) and new-generation (protein) vaccines.
• Gonococcal Infection (Gonorrhea).
o Laboratory surveillance based on whole-genome sequencing and its application in Public Health.
o Study and characterization of antimicrobial resistance mechanisms.
• Listeriosis.
o Laboratory surveillance based on whole-genome sequencing and its application in Public Health.
• Pertussis.
o Development and application of molecular techniques for the diagnosis and characterization of Bordetella pertussis, B. parapertussis, B. holmessi, and B. bronchiseptica.
Neumococos
Vigilancia epidemiológica de los serotipos y genotipos que causan enfermedad neumocócica invasiva (ENI) en España. Caracterización molecular de factores de virulencia de neumococo. Identificación y caracterización de proteínas de neumococo candidatas a vacuna. Evaluación de mecanismos de evasión de la respuesta inmune en Streptococcus pneumoniae. Impacto de los biofilms bacterianos en la persistencia del tracto respiratorio. Mecanismos de cronicidad de aislados clínicos de neumococo en pacientes con enfermedad pulmonar obstructiva crónica.
Patogénesis e inmunidad viral
A) Desarrollo de metodología point of care frente a hepatitis virales en el reservorio del VIH
El tratamiento precoz de las hepatitis virales reduce el deterioro progresivo del hígado y evita el trasplante hepático. Resulta esencial disponer de métodos diagnóstico rápido, sencillos y coste-efectivos, para el cribado, en la vigilancia epidemiológica y el diagnóstico virológico temprano de enfermedades virales hepáticas. Línea de investigación llevada a cabo en colaboración con el Dr. Ricardo Madrid (BioAssays S.L).
B) Impacto de la coinfección y eliminación de las hepatitis virales en el reservorio del VIH
La coinfección por el VHC impacta en el reservorio del VIH, principal obstáculo para eliminar esta infección. Se realizan distintos abordajes del estudio del reservorio del VIH en pacientes VIH+ con distinta exposición al VHC, y tras su eliminación espontánea o con antivirales de acción directa, con el objetivo de identificar y proponer nuevas estrategias de eliminación/curación del VIH. Esta línea de Investigación se desarrolla en el seno del Grupo Multidisciplinar COVIHEP (COinfección por VIH y HEPatitis).
C) Identificación de marcadores de senescencia inducida por virus y estrategias paliativas
Las infecciones virales inducen una senescencia acelerada cuyo impacto afecta a la evolución de la enfermedad y a posibles comorbilidades. Nuestro objetivo es profundizar en los mecanismos que desencadenan la inmunosenescencia y estrés oxidativo asociado a infecciones virales e identificar nuevas estrategias terapéuticas que palien el envejecimiento prematuro en estos pacientes.
D) Impacto de SARS-CoV-2 en la infección por el VIH y hepatitis virales
Se desconocen las complicaciones a largo plazo de la infección por SARS-CoV-2 en personas que viven con VIH y/o hepatitis virales que podrían experimentar un desarrollo clínico de la enfermedad más desfavorable. La identificación de biomarcadores de gravedad no invasivos (como en sangre/plasma) resulta de especial interés en estos pacientes.
E) Origen y Epidemiología de la enfermedad hepática
Estudio del origen y la dinámica de transmisión espacio-temporal de los virus hepáticos, clave para el entendimiento de su evolución y propagación, así como en el análisis de la carga global de las enfermedades, lo que podría ayudar a desarrollar programas de Salud Pública encaminados a prevenir y frenar su transmisión.
F) Impacto de la viremia de bajo grado del VIH
Se desconoce tanto el origen como los mecanismos de la viremia de bajo grado, presente entre el 3 y 16% que las personas que viven con VIH. Su presencia podría desembocar en un mayor riesgo de sufrir comorbilidades relacionadas con enfermedades cardiovasculares, cáncer y trastornos metabólicos.
G) Calidad del aire y su impacto en poblaciones vulnerables
La contaminación del aire agrava las patologías infecciosas y la salud cardiovascular y respiratoria. La evolución de la enfermedad en personas con enfermedades crónicas con VIH y hepatitis puede verse agravada tras la inhalación continua de contaminantes ambientales. Línea de investigación llevada a cabo en colaboración con el CNSA y el CNE del ISCIII.
H) Coinfección por VHE y protistas entéricos en el reservorio humano y animal: vigilancia e investigación
La coinfección entre virus y protistas entéricos podría influir en la cotransmisión y patogenicidad de dichas especies. Línea de investigación, bajo el concepto “One Health” que se centra en la vigilancia y estudio de la coinfección del VHE y protistas entéricos. Colaboración con el grupo multidisciplinar COHEPROEN (COinfección HEpatitis y PROtistas ENtéricos).
Publicaciones destacadas
Evidence for Suppression of Onchocerciasis Transmission in Bioko Island, Equatorial Guinea
Moya L, Herrador Z, Ta-Tang TH, Rubio JM, Perteguer MJ, Hernandez-González A, García B, Nguema R, Nguema J, Ncog P, Garate T, Benito A, Sima A and Aparicio P. Evidence for Suppression of Onchocerciasis Transmission in Bioko Island, Equatorial Guinea.PLoS Negl Trop Dis, 2016; 10(7): e0004829.
PUBMED DOILAMP kit for diagnosis of non-falciparum malaria in Plasmodium ovale infected patients
Cuadros J, Martin Ramírez A, González IJ, Ding XC, Perez Tanoira R, Rojo-Marcos G, Gómez-Herruz P, Rubio JM. LAMP kit for diagnosis of non-falciparum malaria in Plasmodium ovale infected patients. Malar J. 2017 Jan 7;16(1):20.
PUBMED DOIPlasmodium species differentiation by non-expert on-line volunteers for remote malaria field diagnosis
Ortiz-Ruiz A, Postigo M, Gil-Casanova S, Cuadrado D, Bautista JM, Rubio JM, Luengo-Oroz M, Linares M. Plasmodium species differentiation by non-expert on-line volunteers for remote malaria field diagnosis. Malar J. 2018 Jan 30;17(1):54.
PUBMED DOIStudy of the diagnostic accuracy of microbiological techniques in the diagnosis of malaria in the immigrant population in Madrid
Martín-Díaz A, Rubio JM, Herrero-Martínez JM, Lizasoain M, Ruiz-Giardin JM, Jaqueti J, Cuadros J, Rojo-Marcos G, Martín-Rabadán P, Calderón M, Campelo C, Velasco M, Pérez-Ayala A. Study of the diagnostic accuracy of microbiological techniques in the diagnosis of malaria in the immigrant population in Madrid. Malar J. 2018 Aug 29;17(1):314.
PUBMED DOIContent with Investigacion .
-

Almudena Cascajero Díaz
Técnico de laboratorio
ORCID code: 0000-0002-9654-3100
Técnico Superior de Actividades Técnicas y Profesionales (Unidades de Inmunopatología del SIDA y Legionella, Centro Nacional de Microbiología). Clinical Diagnostic Laboratory Technician by IES Renacimiento de Madrid.
Experience in cloning techniques and characterization of neutralizing antibodies and participation in different projects on the pathogenesis of HIV by studying the viral envelope and the mechanisms of resistance to antiretroviral drugs. This experience has subsequently allowed me to participate in 5 multicenter clinical studies studying the immune response against different variants of SARS-CoV-2.
Since 2021, I also participate as a laboratory technician in the Legionella Unit as a support to the Spanish National Health System through the microbiological surveillance of the disease to contribute to the prevention and control of legionellosis.
-
-
Paloma Jiménez Santana
Técnico de laboratorio contratado
-

Javier García Pérez
Investigador Doctor
ORCID code: 0000-0001-7551-7803
Graduated in Biochemistry (1999) and Molecular Biology (2000) from the Autonomous University of Madrid (UAM), he obtained a predoctoral fellowship “ISCIII” in the AIDS Immunopathology laboratory, where he developed new techniques based on recombinant viruses. His doctoral thesis focused on the application of this technological development to the study of the replicative capacity of HIV-1 and its resistance to antiretroviral drugs, obtaining the degree of Doctor of Science from the UAM in 2007.
Thanks to a short postdoc in 2008 and several stays between 2009 and 2015 at the Viral Pathogenesis Unit of the Institut Pasteur in Paris he extended his training in the study of HIV-1 envelope and tropism. Between 2015 and 2019 he rejoins the AIDS Immunopathology Unit at ISCIII, focusing his work on the study of the functional capacity of founder viruses, as well as variants of the virus with interest in Public Health due to its recent expansion in our country. He is currently leading a project on the study of a mutation in transportin 3 observed in patients with a very rare muscular dystrophy (LGMDD2) that confers protection against HIV-1 infection.
During the last 5 years he combines this activity in HIV-1 with the participation and leadership of different clinical trials and studies investigating the immunity generated in people vaccinated against SARS-CoV-2 infection.
Since 2024 he is a “Investigador Doctor fuera de Convenio” at the Spanish National Centre of Microbiology and he currently coordinates together with Dr. Francisco Díez Fuertes the AIDS Immunopathology Unit.
-

Francisco Díez Fuertes
Investigador Doctor Indefinido
ORCID code: 0000-0003-2413-9229
Degree in Biology from the University of León, PhD specialized in molecular virology from the Complutense University of Madrid in 2010 and master's degree in bioinformatics and computational biology from the same university in 2012. He has done research stays at University of Illinois at Urbana Champaign (USA) in 2010, Nebraska Center for Virology (USA) in 2011, Institut Pasteur (France) in 2013 and J. Craig Venter Institute (USA) in 2015-2016.
He joined the AIDS Immunopathology Unit in 2013 with a contract from the “Sara Borrell” postdoctoral program. After a period at the August Pi i Sunyer Biomedical Research Institute in Barcelona he rejoins the AIDS Immunopathology Unit in 2020 as a PhD researcher.
His lines of research have focused on the genomic and transcriptomic characterization of extreme phenotypes in HIV-1 infection, including long-term non-progressors and elite controllers. He collaborates with other laboratories of the center in the analysis of outbreaks caused by viruses with interest in Public Health, as well as in evolutionary studies on genomic epidemiology. Since 2020 he has led different clinical studies on COVID-19. Currently, he combines omics sciences with different bioinformatics tools to answer different scientific questions in the field of virology, especially in HIV-1 and SARS-CoV-2 research. He currently coordinates together with Dr. Javier García Pérez the AIDS Immunopathology Unit.
-
Mercedes Bermejo Herrero
Investigadora post-doctoral contratada
ORCID code: 0000-0001-9909-8578
Degree and PhD in Biological Sciences (Biochemistry and Molecular Biology) from the Autonoma University of Madrid. Her doctoral thesis studied the expression of CXCR4 and SDF-1/CXCL12 in lymphocytes and dendritic cells and their implications in HIV-1 infection.
She has completed internships in various laboratories: the Immunology Department of the Gregorio Marañón University Hospital in Madrid, the Research Center of the 12 de Octubre University Hospital in Madrid (where she was head of the flow cytometry service) and is currently at the CNM (National Research Center) of the Carlos III Health Institute.
Her research interests have focused on the study of HIV biology and its interaction with the immune system. She has currently participated in clinical trials, CombiVacs and ENE-Covid Senior, and in collaboration with Hipra.
-

Nuria González Fernández
Investigadora Contratada indefinida
ORCID code: 0000-0002-0087-5144
She completed her PhD in 2007 (Universidad Autónoma de Madrid), focused on the development of an envelope recombinant virus system to characterize HIV-1 tropism, as well as on the study of the role of the chemokine CXCL12 in virus propagation at the infectious synapse. Part of this work was carried out in the laboratory of Dr. Quentin Sattentau at the University of Oxford.
During her postdoctoral period, she expanded her research on the mechanisms of HIV entry and specialized in the study of the neutralizing response. She developed a system to measure neutralizing activity, which has been used in clinical trials of HIV vaccine candidates. During a stay at the Vaccine Research Center, NIH (USA), she acquired experience in various techniques for the characterization of broadly neutralizing antibodies, leading to new collaborations and research projects, which she is currently developing in the AIDS Immunopathology Unit of the Carlos III Health Institute.
She has participated in research networks such as EAVI2020 (co-PI), CIBERINFEC, RIS and EUROPRISE (EU). Since 2014 she is a professor of the Master in Microbiology applied to Public Health and Infectious Diseases Research at the University of the University of Alcalá and, since 2023, of the Master in Human Immunodeficiency Virus Infection at the University Rey Juan Carlos.
-

Rubén Ayala Suárez
Técnico Superior Especializado OPI
ORCID code: 0000-0002-1271-646.
Graduated in Biotechnology from the University of Cadiz (2015), Master in Microbiology of Infectious Diseases (2016) and PhD in Functional Biology from the University of Alcalá (2023). He carried out his PhD Thesis at the AIDS Immunopathology laboratory (CNM) on post-translational epigenetic mechanisms of natural control of HIV infection. In the same period, he completed a Diploma in Bioinformatics at Pablo de Olavide University (2021).
In 2023 he joined as a postdoctoral researcher in the HIV and AIDS research group at the August Pi i Sunyer Biomedical Research Institute (Barcelona), where he worked on the relationship of HIV and senescence until his incorporation as a Técnico Superior Especializado in the AIDS Immunopathology unit of the Spanish National Center of Microbiology (ISCIII) in 2025.
The main research projects in which he participates focus on resistance and natural control to HIV infection, as well as the evaluation of the immune response in vaccine trials, using mainly bioinformatics techniques focused on massive sequencing (RNA-Seq, single-cell, genome sequencing), the application of biostatistics and machine learning in data management.
-

Manuela Beltrán Vicente
Técnico de Laboratorio Indefinido
ORCID code: 0000-0001-6185-2280
Senior Technician of Technical and Professional Activities (AIDS Immunopathology Unit, Spanish National Center of Microbiology).
Clinical Analysis Laboratory Specialist Technician by IES Las Musas (Madrid, 1996). Demonstrated experience in the development of strategies against HIV, focused on the screening of compounds of both natural and synthetic origin with antiviral activity and identification and evaluation of potential therapeutic agents, as well as the screening of serological samples for the study of immunity for the identification of possible strategies for the development of vaccines against HIV. -

Silvia Jara Herrera
Técnico de Laboratorio Contratado CIBERINFEC
ORCID code: 0009-0001-2842-2040
Clinical and Biomedical Diagnostic Laboratory Technician.
She is currently working in the AIDS Immunopathology Unit of the Spanish National Center of Microbiology (ISCIII) with a contract through the Spanish Biomedical Research Networking Centre in Infectious Diseases (CIBER-INFEC).
She worked from March 2020 to September 2024 at the Department of Animal Health (Faculty of Veterinary Medicine) of the Universidad Complutense de Madrid.
She has experience in serological techniques (ELISA, Western Blot and IFA), cell culture and molecular biology.
-

Irene Díaz Marín
Técnico de laboratorio contratado
Clinical and Biomedical Diagnostics laboratory technician by CIFP Politécnico de Murcia-CESUR and graduated in Journalism from the Complutense University of Madrid.
She is currently at the AIDS Immunopathology Unit of the Spanish National Center of Microbiology with a contract of the “Garantía Juvenil” program (Community of Madrid), where she performs technical tasks in several research projects about HIV-1 and COVID-19.
-
José Alcamí Pertejo
Profesor de Investigación
ORCID code: 0000-0003-0023-7377
Degree in Medicine from the Universidad Autónoma and Doctor of Medicine from the Universidad Complutense de Madrid. Specialist in Internal Medicine at Hospital 12 de Octubre (1982-1986). Training in immunology by means of a Research Staff grant (1986-1988). Research associate at the Viral Immunology Unit of the Pasteur Institute in Paris (1988-1992) where he obtained a Master in Immunopathology from the Institute. Research Professor since 2015, he directed the AIDS Immunopathology Unit at the National Microbiology Center since 2000. Coordinator since 2003 of the Spanish AIDS Research Network, he participates as group leader in European networks of excellence whose objective is the development of new vaccines, drugs and microbicides against HIV/AIDS: EUROPRISE, AIM-HIV, CHAARM and EAVI2020. Since 2019 he has been the Scientific Director of the HIV Unit at the Hospital Clinic of Barcelona. He has been Professor of Immunology and Virology at the European University of Madrid between 2012 and 2014 and Director of the Master in Public Health and Research in Infectious Diseases at the University of Alcalá de Henares from 2014 to 2023.
Author of more than 200 scientific articles in high impact journals such as Nature, Nature Reviews in Microbiology, Nature Medicine, Lancet and Journal of Clinical Investigation and more than 80 chapters in books. Scientific disseminator through his YouTube channel and on the X platform. He has been principal investigator of more than 50 research projects, including European projects and an American NIH project.
Consultant for FIS and ANEP since 1992, member of the scientific council of the French Evaluation Agency in AIDS between 2008 and 2014, evaluator of EU FP6, FP7 and H2020 programs, member of the external scientific council of the Global Health Institute (Hospital Ramón y Cajal), scientific collaborator of the EMA and AEMPS where he has been part of the biotechnology, antivirals and vaccines committees. Scientific member of the EU Vaccelerate consortium and associate editor of the Journal of Virology, Frontiers in Cellular and Infection Microbiology and HIV medicine.
-
Laura Capa Muñoz
Investigadora post-doctoral contratada
ORCID code: 0000-0002-0234-331X
Degree in Biological Sciences from the Universidad Autónoma de Madrid and PhD from the Universidad Complutense de Madrid, she has a master's degree in AIDS (Universidad Complutense de Madrid) and a master's degree in HIV infection (Universidad Rey Juan Carlos de Madrid).
Professional activity developed mainly in the study of infectious diseases, both in the field of basic research in public research centers and in the pharmaceutical industry, as well as in the field of public health and scientific management. She has worked in the international response to the HIV pandemic, representing the Ministry of Health as an expert in meetings of the European Commission and collaborated with the WHO. At the Instituto de Salud Carlos III, she has led the scientific management of national and European projects in the AIDS Immunopathology Unit and has been part of the Institute's Data Protection Working Group. Currently, she continues to coordinate the Cohort of Long-Term Non-Progressing Patients created by the Spanish AIDS Research Network (RIS), is part of the coordination team of the PhD Program in Biomedical Sciences and Public Health IMIENS-UNED-ISCIII and of the Institute's Working Group on Equality.
List of staff
Información adicional
The researchers of the Viral Infection and Immunity Unit (UIVI) are part of the CIBER de Infectious Diseases (CIBERINFEC) as an independent group (https://www.ciberinfec.es/grupos/grupo-de-investigacion?id=27501). The UIVI studies the immunopathology of clinically relevant infections in humans, such as chronic viral hepatitis (Hepatitis B, C and D), HIV, and SARS-CoV-2, and their impact on the clinical evolution of infected patients. We also analyse the evolution of the patient after controlling viral replication or after eliminating the virus spontaneously or by antiviral treatment.
The group focuses mainly on translational research in which collaborating clinical groups also participate. On the one hand, ‘omics’ techniques such as genomics, transcriptomics, proteomics, metabolomics, epigenetics and metagenomics are used, which, depending on the type of study, are targeted or not. On the other hand, specific laboratory assays designed in-house, such as PCR, RT-PCR, immunoassays for virus titration and neutralisation, production of monoclonal antibodies, among others, are carried out. With the molecular data obtained from patient samples, we perform bioinformatics/statistical analyses, analysing their association with the clinical condition of the patients and their subsequent evolution.