Bacterial Genetics
Research Lines
Content with Investigacion .
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
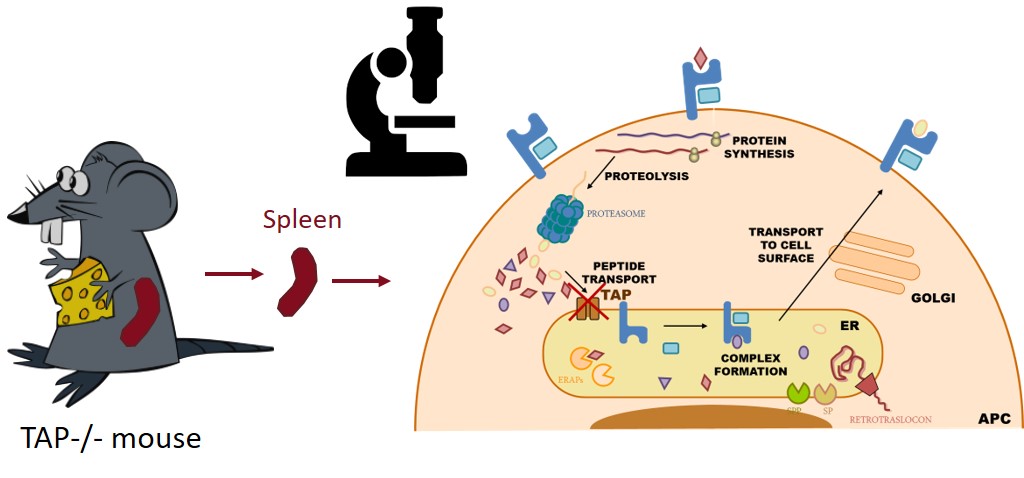
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
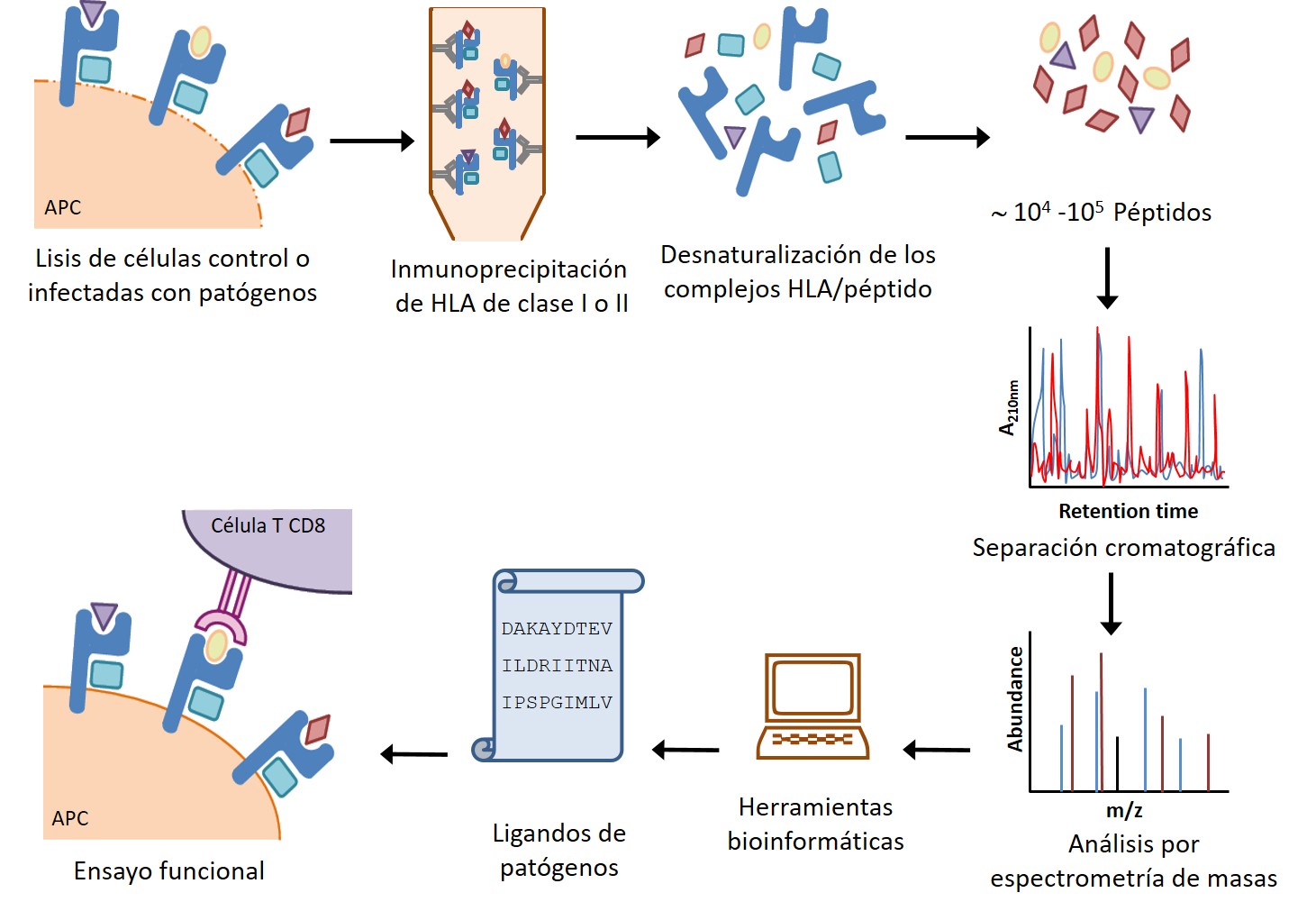
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

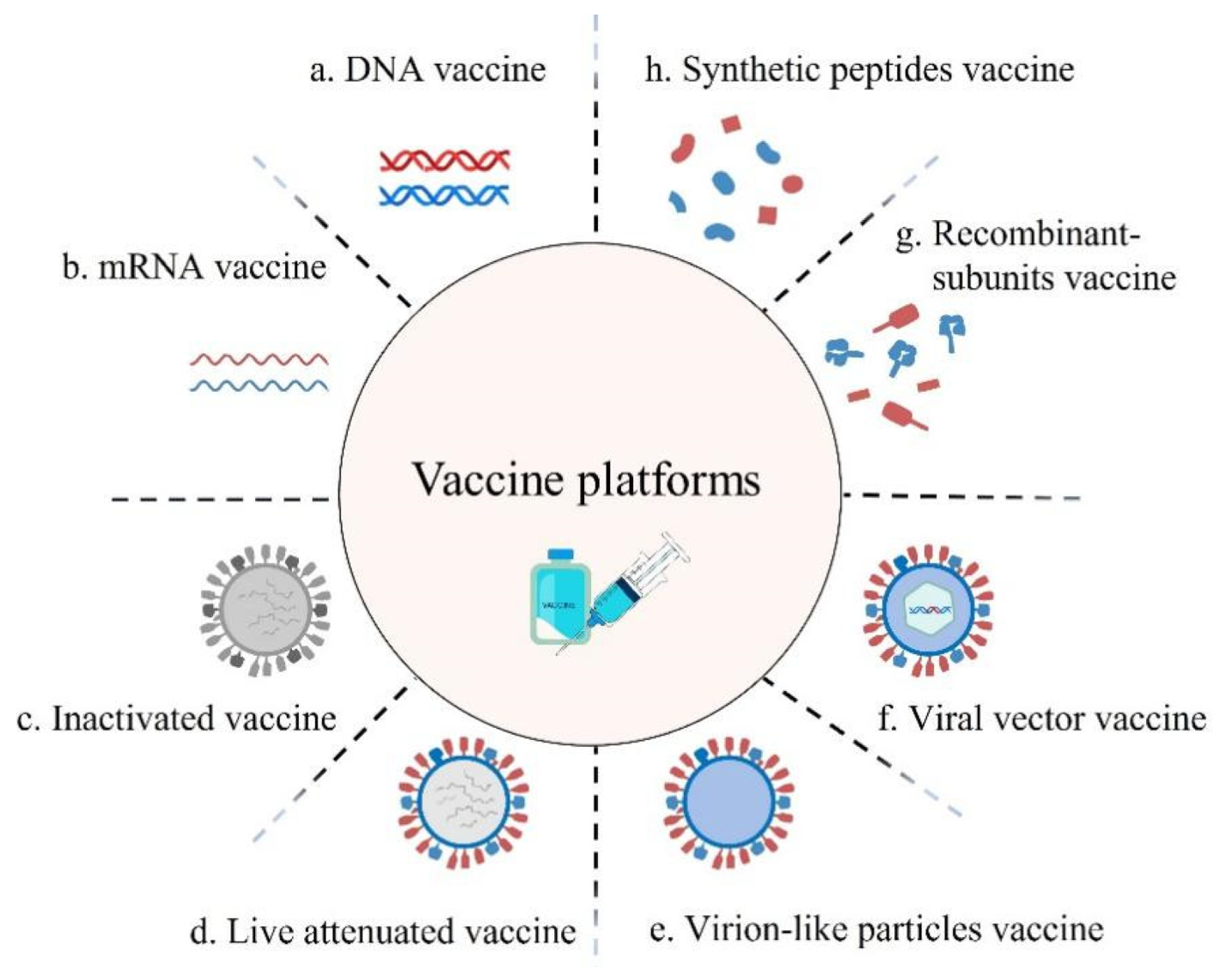
* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Isolation of Functional SARS-CoV-2 Antigen-Specific T-Cells with Specific Viral Cytotoxic Activity for Adoptive Therapy of COVID-19. García-Ríos, E.; Leivas, A.; Mancebo, F.J.; Sánchez-Vega, L.; Lanzarot, D.; Aguado, J.M.; Martínez-López, J.; Paciello, M.L.; Pérez-Romero, P. Biomedicines 2022, 10, 630. doi: 10.3390/biomedicines10030630.
Isolation of Functional SARS-CoV-2 Antigen-Specific T-Cells with Specific Viral Cytotoxic Activity for Adoptive Therapy of COVID-19. García-Ríos, E.; Leivas, A.; Mancebo, F.J.; Sánchez-Vega, L.; Lanzarot, D.; Aguado, J.M.; Martínez-López, J.; Paciello, M.L.; Pérez-Romero, P. Biomedicines 2022, 10, 630. doi: 10.3390/biomedicines10030630.
Deciphering the Potential Coding of Human Cytomegalovirus: New Predicted Transmembrane Proteome. Mancebo, F.J., Parras-Moltó, M., García-Ríos, E., Pérez-Romero, P. International Journal of Molecular Sciences, 2022, 23(5), 2768. doi: 10.3390/ijms23052768.
Deciphering the Potential Coding of Human Cytomegalovirus: New Predicted Transmembrane Proteome. Mancebo, F.J., Parras-Moltó, M., García-Ríos, E., Pérez-Romero, P. International Journal of Molecular Sciences, 2022, 23(5), 2768. doi: 10.3390/ijms23052768.
Detection of cytomegalovirus drug resistance mutations in solid organ transplant recipients with suspected resistance
Cross-Recognition of SARS-CoV-2 B-Cell Epitopes with Other Betacoronavirus Nucleoproteins. Tajuelo, A.; López-Siles, M.; Más, V.; Pérez-Romero, P.; Aguado, J.M.; Briz, V.; McConnell, M.J.; Martín-Galiano, A.J.; López, D. Int. J. Mol. Sci. 2022, 23, 2977. doi: 10.3390/ijms23062977.
PUBMEDDetection of cytomegalovirus drug resistance mutations in solid organ transplant recipients with suspected resistance
Immunogenicity of Anti-SARS-CoV-2 Vaccines in Common Variable Immunodeficiency. Arroyo-Sánchez D, Cabrera-Marante O, Laguna-Goya R, Almendro-Vázquez P, Carretero O, Gil-Etayo FJ, Suàrez-Fernández P, Pérez-Romero, P, Rodríguez de Frías E, Serrano A, Allende LM, Pleguezuelo D, Paz-Artal E. J Clin Immunol. 2022 Feb;42(2):240-252. doi: 10.1007/s10875-021-01174-5. PMID: 34787773.
PUBMEDOptimization of a Lambda-RED Recombination Method for Rapid Gene Deletion in Human Cytomegalovirus
Optimization of a Lambda-RED Recombination Method for Rapid Gene Deletion in Human Cytomegalovirus. García-Ríos E, Gata-de-Benito J, López-Siles M, McConnell MJ, Pérez-Romero, P. Int J Mol Sci. 2021 Sep 29;22(19):10558. doi: 10.3390/ijms221910558. PMID: 34638896.
PUBMEDCirculatory follicular helper T lymphocytes associate with lower incidence of CMV infection in kidney transplant recipients
Circulatory follicular helper T lymphocytes associate with lower incidence of CMV infection in kidney transplant recipients. Suàrez-Fernández P, Utrero-Rico A, Sandonis V, García-Ríos E, Arroyo-Sánchez D, Fernández-Ruiz M, Andrés A, Polanco N, González-Cuadrado C, Almendro-Vázquez P, Pérez-Romero P, Aguado JM, Paz-Artal E, Laguna-Goya R. Am J Transplant. 2021 Dec;21(12):3946-3957. doi: 10.1111/ajt.16725. PMID: 34153157.
PUBMEDIs It Feasible to Use CMV-Specific T-Cell Adoptive Transfer as Treatment Against Infection in SOT Recipients?
Is It Feasible to Use CMV-Specific T-Cell Adoptive Transfer as Treatment Against Infection in SOT Recipients? García-Ríos E, Nuévalos M, Mancebo FJ, Pérez-Romero P. Front Immunol. 2021 Apr 23;12:657144. doi: 10.3389/fimmu.2021.657144. PMID: 33968058.
PUBMEDCytotoxic cell populations developed during treatment with tyrosine kinase inhibitors protect autologous CD4+ T cells from HIV-1 infection
Cytotoxic cell populations developed during treatment with tyrosine kinase inhibitors protect autologous CD4+ T cells from HIV-1 infection. Vigón L, Rodríguez-Mora S, Luna A, Sandonís V, Mateos E, Bautista G, Steegmann JL, Climent N, Plana M, Pérez-Romero P, de Ory F, Alcamí J, García-Gutierrez V, Planelles V, López-Huertas MR, Coiras M. Biochem Pharmacol. 2020 Aug 20;182:114203. doi: 10.1016/j.bcp.2020.114203. PMID: 32828803
PUBMEDRole of Neutralizing Antibodies in CMV Infection: Implications for New Therapeutic Approaches
Role of Neutralizing Antibodies in CMV Infection: Implications for New Therapeutic Approaches. Sandonís V, García-Ríos E, McConnell MJ, Pérez-Romero P.Sandonís V, et al. Trends Microbiol. 2020 Nov;28(11):900-912. doi: 10.1016/j.tim.2020.04.003. PMID: 32448762 Review.
PUBMEDPre-existing Hemagglutinin Stalk Antibodies Correlate with Protection of Lower Respiratory Symptoms in Flu-Infected Transplant Patients
Pre-existing Hemagglutinin Stalk Antibodies Correlate with Protection of Lower Respiratory Symptoms in Flu-Infected Transplant Patients. Aydillo T, Escalera A, Strohmeier S, Aslam S, Sanchez-Cespedes J, Ayllon J, Roca-Oporto C, Pérez-Romero P, Montejo M, Gavalda J, Munoz P, Lopez-Medrano F, Carratala J, Krammer F, García-Sastre A, Cordero E. Cell Rep Med. 2020 Nov 3;1(8):100130. doi: 10.1016/j.xcrm.2020.100130. PMID: 33294855
PUBMEDEffect of Influenza Vaccination Inducing Antibody Mediated Rejection in Solid Organ Transplant Recipients. Cordero E, Bulnes-Ramos A, Aguilar-Guisado M, González Escribano F, Olivas I, Torre-Cisneros J, Gavaldá J, Aydillo T, Moreno A, Montejo M, Fariñas MC, Carratalá J, Muñoz P, Blanes M, Fortún J, Suárez-Benjumea A, López-Medrano F, Roca C, Lara R, Pérez-Romero P. Front Immunol. 2020 Oct 6;11:1917. doi: 10.3389/fimmu.2020.01917. PMID: 33123119
Effect of Influenza Vaccination Inducing Antibody Mediated Rejection in Solid Organ Transplant Recipients. Cordero E, Bulnes-Ramos A, Aguilar-Guisado M, González Escribano F, Olivas I, Torre-Cisneros J, Gavaldá J, Aydillo T, Moreno A, Montejo M, Fariñas MC, Carratalá J, Muñoz P, Blanes M, Fortún J, Suárez-Benjumea A, López-Medrano F, Roca C, Lara R, Pérez-Romero P. Front Immunol. 2020 Oct 6;11:1917. doi: 10.3389/fimmu.2020.01917. PMID: 33123119
Humoral response to natural influenza infection in solid organ transplant recipients
Humoral response to natural influenza infection in solid organ transplant recipients. Hirzel C, Ferreira VH, L'Huillier AG, Hoschler K, Cordero E, Limaye AP, Englund JA, Reid G, Humar A, Kumar D; Influenza in Transplant Study Group.Hirzel C, et al. Am J Transplant. 2019 Aug;19(8):2318-2328. doi: 10.1111/ajt.15296. Epub 2019 Mar 18.Am J Transplant. 2019. PMID: 30748090 Clinical Trial.
PUBMEDA 5-Year Prospective Multicenter Evaluation of Influenza Infection in Transplant Recipients
A 5-Year Prospective Multicenter Evaluation of Influenza Infection in Transplant Recipients. Kumar D, Ferreira VH, Blumberg E, Silveira F, Cordero E, Perez-Romero P, Aydillo T, Danziger-Isakov L, Limaye AP, Carratala J, Munoz P, Montejo M, Lopez-Medrano F, Farinas MC, Gavalda J, Moreno A, Levi M, Fortun J, Torre-Cisneros J, Englund JA, Natori Y, Husain S, Reid G, Sharma TS, Humar A.Kumar D, et al. Clin Infect Dis. 2018 Oct 15;67(9):1322-1329. doi: 10.1093/cid/ciy294.Clin Infect Dis. 2018. PMID: 29635437 Clinical Trial.
PUBMEDImpact of pretransplant CMV-specific T-cell immune response in the control of CMV infection after solid organ transplantation: a prospective cohort study
Impact of pretransplant CMV-specific T-cell immune response in the control of CMV infection after solid organ transplantation: a prospective cohort study. Molina-Ortega A, Martín-Gandul C, Mena-Romo JD, Rodríguez-Hernández MJ, Suñer M, Bernal C, Sánchez M, Sánchez-Céspedes J, Pérez Romero P, Cordero E.Molina-Ortega A, et al. Clin Microbiol Infect. 2019 Jun;25(6):753-758. doi: 10.1016/j.cmi.2018.09.019. PMID: 30292792 Clinical Trial.
PUBMEDTwo Doses of Inactivated Influenza Vaccine Improve Immune Response in Solid Organ Transplant Recipients: Results of TRANSGRIPE 1-2, a Randomized Controlled Clinical Trial.
Two Doses of Inactivated Influenza Vaccine Improve Immune Response in Solid Organ Transplant Recipients: Results of TRANSGRIPE 1-2, a Randomized Controlled Clinical Trial. Cordero E, Roca-Oporto C, Bulnes-Ramos A, Aydillo T, Gavaldà J, Moreno A, Torre-Cisneros J, Montejo JM, Fortun J, Muñoz P, Sabé N, Fariñas MC, Blanes-Julia M, López-Medrano F, Suárez-Benjumea A, Martinez-Atienza J, Rosso-Fernández C, Pérez-Romero P. Clin Infect Dis. 2017 Apr 1;64(7):829-838. doi: 10.1093/cid/ciw855.Clin Infect Dis. 2017. PMID: 28362949 Clinical Trial.
PUBMEDUse of antibodies neutralizing epithelial cell infection to diagnose patients at risk for CMV Disease after transplantation
Use of antibodies neutralizing epithelial cell infection to diagnose patients at risk for CMV Disease after transplantation. Blanco-Lobo P, Cordero E, Martín-Gandul C, Gentil MA, Suárez-Artacho G, Sobrino M, Aznar J, Pérez-Romero P.Blanco-Lobo P, et al. J Infect. 2016 May;72(5):597-607. doi: 10.1016/j.jinf.2016.02.008. Epub 2016 Feb 24.J Infect. 2016. PMID: 26920791 Clinical Trial.
PUBMEDIdentification and Analysis of Unstructured, Linear B-Cell Epitopes in SARS-CoV-2 Virion Proteins for Vaccine Development
Identification and Analysis of Unstructured, Linear B-Cell Epitopes in SARS-CoV-2 Virion Proteins for Vaccine Development. Corral-Lugo A, López-Siles M, López D, McConnell MJ, Martin-Galiano AJ. Vaccines. 2020 Jul 20;8(3):397. doi: 10.3390/vaccines8030397.
PUBMEDUsing Omics Technologies and Systems Biology to Identify Epitope Targets for the Development of Monoclonal Antibodies Against Antibiotic-Resistant Bacteria
Using Omics Technologies and Systems Biology to Identify Epitope Targets for the Development of Monoclonal Antibodies Against Antibiotic-Resistant Bacteria. Martín-Galiano AJ, McConnell MJ.Front Immunol. 2019 Dec 10;10:2841. doi: 10.3389/fimmu.2019.02841. eCollection 2019.
PUBMEDA lipopolysaccharide-free outer membrane vesicle vaccine protects against Acinetobacter baumannii infection
A lipopolysaccharide-free outer membrane vesicle vaccine protects against Acinetobacter baumannii infection. Pulido MR, García-Quintanilla M, Pachón J, McConnell MJ.Vaccine. 2020 Jan 22;38(4):719-724. doi: 10.1016/j.vaccine.2019.11.043.
PUBMEDA Live Salmonella Vaccine Delivering PcrV through the Type III Secretion System Protects against Pseudomonas aeruginosa.
A Live Salmonella Vaccine Delivering PcrV through the Type III Secretion System Protects against Pseudomonas aeruginosa. Aguilera-Herce J, García-Quintanilla M, Romero-Flores R, McConnell MJ, Ramos-Morales F. mSphere. 2019 Apr 17;4(2):e00116-19. doi: 10.1128/mSphere.00116-19.
PUBMEDAdditional Information
Streptococcus pneumoniae is a human pathogen that, despite the development of vaccines, continues to be an important cause of mortality and morbidity. We investigate the mechanisms of antibiotic resistance in this bacterium. On the one hand by identifying new therapeutic targets and on the other hand by investigating the molecular basis of the action of antibiotics already used in clinical practice (the fluoroquinolones levofloxacin and moxifloxacin) or not yet used (seconeolitsine). For this purpose, we used a multidisciplinary analysis involving genomics, transcriptomics and proteomics to understand the organization of the S. pneumoniae chromosome and the identification of the factors that stabilize this organization, including ncRNAs. Changes in the level of global supercoiling, either by inhibition of gyrase (decrease) or by inhibition of topoisomerase I (increase) alter the transcriptome. The modulated genes are located in domains, whose genes show specific functional characteristics. The aim is to identify new factors essential for S. pneumoniae physiology and to characterize transcriptional regulation in response to topological stress. In addition, RNA interference technology and CRISPR systems will be used as novel antibacterials. These studies will establish the bases for translational research aimed at the development of new therapeutic targets for the treatment of pneumococcal diseases.
Streptococcus pneumoniae is a human pathogen that, despite the development of vaccines, continues to be an important cause of mortality and morbidity. We investigate the mechanisms of antibiotic resistance in this bacterium. On the one hand by identifying new therapeutic targets and on the other hand by investigating the molecular basis of the action of antibiotics already used in clinical practice (the fluoroquinolones levofloxacin and moxifloxacin) or not yet used (seconeolitsine). For this purpose, we used a multidisciplinary analysis involving genomics, transcriptomics and proteomics to understand the organization of the S. pneumoniae chromosome and the identification of the factors that stabilize this organization, including ncRNAs. Changes in the level of global supercoiling, either by inhibition of gyrase (decrease) or by inhibition of topoisomerase I (increase) alter the transcriptome. The modulated genes are located in domains, whose genes show specific functional characteristics. The aim is to identify new factors essential for S. pneumoniae physiology and to characterize transcriptional regulation in response to topological stress. In addition, RNA interference technology and CRISPR systems will be used as novel antibacterials. These studies will establish the bases for translational research aimed at the development of new therapeutic targets for the treatment of pneumococcal diseases.