Desde el ISCIII mostramos nuestra solidaridad con todas las personas afectadas por el desastre de la DANA
Todo nuestro apoyo en estos momentos tan difíciles
Actualidad
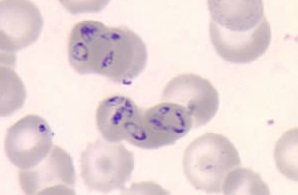
Nuevos avances en el estudio de la babesiosis humana gracias a tres artículos sobre su origen, diagnóstico y coinfección
Un equipo del Instituto de Salud Carlos III (ISCIII) ha publicado tres artículos de investigación en torno al estudio de la babesiosis, una infección similar a la malaria, que revelan nuevos conocimientos para seguir mejorando su diagnóstico y tratamiento. Los resultados de su trabajo se han publicado en las revistas PLOS Neglected Tropical Diseases, International Journal of Molecular Sciences y Microorganisms. La babesiosis es una enfermedad que afecta a humanos y animales, provocada por protozoos del género Babesia y transmitida normalmente por la picadura de un tipo de garrapata, llamada Ixodes. Tras la picadura, Babesia infecta a los eritrocitos provocando síntomas que pueden ser leves, pero también complicarse y generar fiebres muy altas y diferentes fallos orgánicos, hasta causar la muerte. Para tratar la babesiosis leve o moderada se utilizan antibióticos de amplio espectro, como la azitromizina, y medicamentos antiprotozoarios como la atovacuona; en casos de infección grave están indicadas la quinina y la clindamicina en combinación con los otros tratamientos y la exanguinotransfusión. La investigación está coordinada desde el Centro Nacional de Microbiología (CNM) del ISCIII, por un equipo liderado por Estrella Montero y Luis Miguel González, que lleva años estudiando la babesiosis humana y que hace dos años participó en un estudio internacional que reveló el primer 'mapa' genómico del parásito causante de la enfermedad. El primero de los estudios se centra en una de las proteínas implicadas en el ciclo celular de uno de los parásitos que causa la enfermedad y que circula por España y Europa, Babesia divergens. Los resultados han permitido conocer mejor el papel de la proteína BdP50 y su asociación con las vesículas extracelulares del parásito durante su ciclo de vida, concretamente en el proceso de infección de los eritrocitos, lo que arroja nueva luz sobre la aparición de la babesiosis y ofrece nuevos conocimientos para investigar nuevas intervenciones terapéuticas. En el segundo de los artículos, se ha utilizado una estrategia de espectrometría de masas multiplataforma para examinar en detalle el metabolismo del mismo agente infeccioso, B. divergens. Este estudio proporciona nuevos datos sobre las rutas metabolómicas del parasito y de los metabolitos que produce durante su propagación y supervivencia en el interior de los eritrocitos humanos, así como sobre las interacciones metabólicas entre esta célula huésped y el parásito. En concreto, se revela que la glucosa y la glutamina, pero no la hipoxantina, son necesarias para su crecimiento y capacidad infecciosa. Finalmente, el tercero de los artículos analiza las complicaciones que pueden sufrir los pacientes con borreliosis de Lyme, -una infección transmitida también por garrapatas que puede afectar a la piel, el sistema nervioso, el corazón y los músculos- especialmente en aquellos que, además, han estado expuestos a infecciones por B. divergens/venatorum. Según sus conclusiones, los pacientes con borreliosis de Lyme que también habían estado expuestos a la infección por Babesia spp. presentan un número significativamente mayor de síntomas cardiorrespiratorios, en comparación con los que sólo habían sido infectados por Borrelia burgdorferi sensu lato, la bacteria causante de la borreliosis de Lyme.. Aitor Gil, Luis Miguel González, Carmen Terrón, Estrella Montero y Javier Sotillo, investigadores del ISCIII y firmantes de los artículos. En conjunto, los hallazgos obtenidos en estos tres estudios complementarios representan un avance integral en el conocimiento de la biología de Babesia y de las interacciones y alteraciones que el parásito provoca en el eritrocito humano. Además, pone de manifiesto las complicaciones clínicas asociadas a la coinfección de la borreliosis de Lyme y la babesiosis humana: "Sin duda estos estudios facilitarán nuevas investigaciones en torno la etiología, el abordaje integral clínico y diagnóstico y el tratamiento de esta enfermedad emergente", concluyen los autores. Referencia de los artículos: • Gonzalez LM, Revuelta B, Gil A, Terrón MC, Sachse MC, Sotillo J, et al. (2025) Elucidating the functional role of the novel BdP50 protein and extracellular vesicles in the human erythrocyte infection by Babesia divergens. PLoS Negl Trop Dis 19(8): e0013401. https://doi.org/10.1371/journal.pntd.0013401. • Fernández-García, M.; Gonzalez, L.M.; Sevilla, E.; Gil, A.; Santos-Oliveira, H.; Revuelta, B.; Barbas, C.; Rey-Stolle, M.F.; Montero, E.; García, A. Application of Multiplatform Mass Spectrometry to the Study of Babesia divergens Metabolism and the Pathogenesis of Human Babesiosis. Int. J. Mol. Sci. 2025, 26, 7677. https://doi.org/10.3390/ijms26167677. • Folgueras, M.; González, L.M.; Gil, A.; Collazos, J.; Rodríguez-Pérez, M.; Pérez-Is, L.; Díaz-Arias, J.; Meana, M.; Revuelta, B.; Gray, J.; et al. Epidemiological, Clinical and Analytical Features in Lyme Borreliosis Patients Seropositive for Babesia divergens/venatorum. Microorganisms 2025, 13, 1383. https://doi.org/10.3390/microorganisms13061383. Más información: - Revelado el primer 'mapa' genómico del parásito causante de la babesiosis humana
Saber más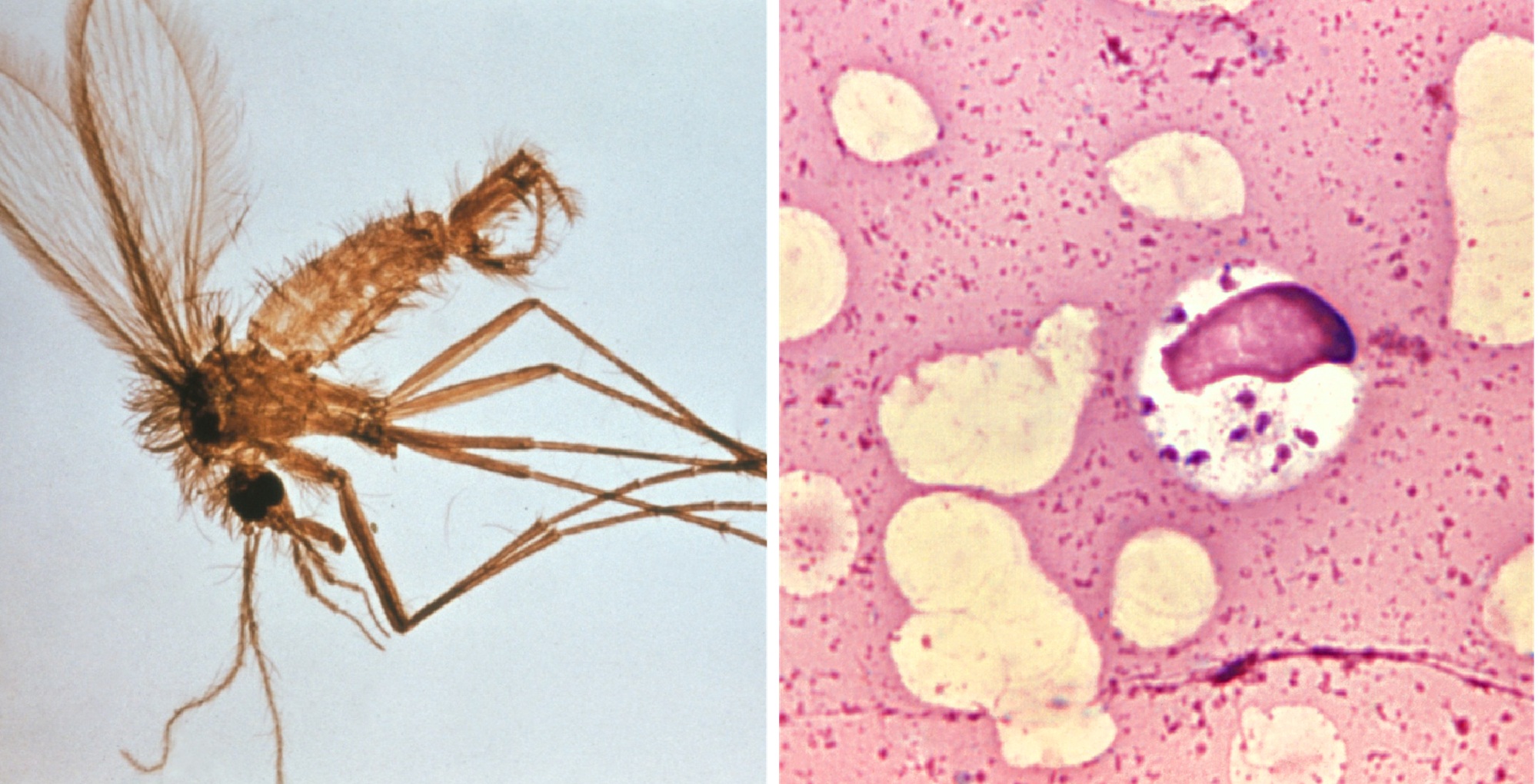
Estudiar las vesículas extracelulares podría facilitar la búsqueda de biomarcadores diagnóstico y terapias en leishmaniasis visceral
Una investigación del Instituto de Salud Carlos III (ISCIII) revela que estudiar las vesículas extracelulares de plasma, estructuras con material genético y proteico liberadas por las células, podría facilitar la identificación de biomarcadores pronósticos en la leishmaniasis visceral, una enfermedad infecciosa desatendida que puede llegar a ser mortal si no se detecta y trata de forma eficaz. El estudio se ha publicado en la revista Frontiers in Immunology. La leishmaniasis visceral está causada por protozoos de la familia Leishmania y se caracteriza por fiebre crónica, agrandamiento del bazo e hígado y pancitopenia. Tiene una prevalencia especialmente importante en pacientes inmunosuprimidos, particularmente en aquellos coinfectados con VIH y en personas con inmunosupresión inducida por tratamientos biológicos como los antagonistas del TNF (anti-TNF). La enfermedad se transmite principalmente a través de la picadura de mosquitos -flebótomos-, que actúan como vectores del parásito. El estudio, llevado a cabo por un equipo del ISCIII en el Centro Nacional de Microbiología (CNM), ha analizado el impacto de la terapia inmunosupresora anti-TNF en la progresión de la leishmaniasis visceral y en la eficacia del tratamiento antiparasitario con antimoniales pentavalentes, utilizando un modelo animal murino. Dos de los autores principales del trabajo son Eugenia Carrillo y Javier Moreno, del CNM-ISCIII. Para realizar esta investigación se han empleado técnicas de proteómica para estudiar vesículas extracelulares procedentes del plasma de ratones infectados con Leishmania infantum. Este trabajo supone una continuación de una línea de investigación del equipo del ISCIII en torno al efecto de diferentes fármacos inmunosupresores en la respuesta inmunitaria en esta enfermedad y en el impacto en la eficacia de su tratamiento. Los resultados obtenidos en el estudio ahora publicado revelan que los ratones tratados con anti-TNF desarrollaron una mayor carga parasitaria en el hígado y una respuesta inmunitaria más debilitada. También se observó una disminución significativa de diversas proteínas, procedentes de vesículas extracelulares plasmáticas, cuya función es clave en procesos de regeneración hepática, respuesta inflamatoria y defensa frente a infecciones. Tras el tratamiento con los antimoniales pentavalentes, en el grupo de animales inmunosuprimidos se logró solo una reducción parcial de la carga parasitaria, acompañada por un aumento de otras proteínas cuya sobreexpresión podría favorecer la persistencia del parásito. Los autores y autoras de la investigación explican que estos hallazgos demuestran que la inmunosupresión con anti-TNF no sólo agrava la enfermedad, sino que también altera profundamente el perfil proteico de las vesículas extracelulares, afectando rutas biológicas esenciales para la recuperación y la eficacia del tratamiento. Según concluyen, "estos resultados recuerdan la importancia de adaptar a cada caso las estrategias clínicas en pacientes inmunosuprimidos, y posiciona a las vesículas extracelulares como una herramienta prometedora para identificar biomarcadores pronósticos y optimizar el manejo terapéutico de la leishmaniasis visceral". • Referencia del artículo: Bernardo L, Montero-Calle A, Solana JC, Lozano-Rendal M, Torres A, Sánchez C, Barderas R, Moreno J and Carrillo E (2025) Protein dysregulation during Leishmania infantum infection in anti-TNF immunosuppressed mice revealed through quantitative proteomics analysis of extracellular vesicles. Front. Immunol. 16:1634080. doi: 10.3389/fimmu.2025.1634080. De izquierda a derecha, el equipo de investigación que ha llevado a cabo el estudio: Javier Moreno, Alba Lain, Arantxa Marco, Lorena Bernardo, Ana Torres, Girma Shumie (Armauer Hansen Research Institute- AHRI, Addis Abeba, Etiopía), Carmen Sánchez, José Carlos Solana, Marina Lozano y Eugenia Carrillo, en el Centro Nacional de Microbiología del ISCIII.
Saber más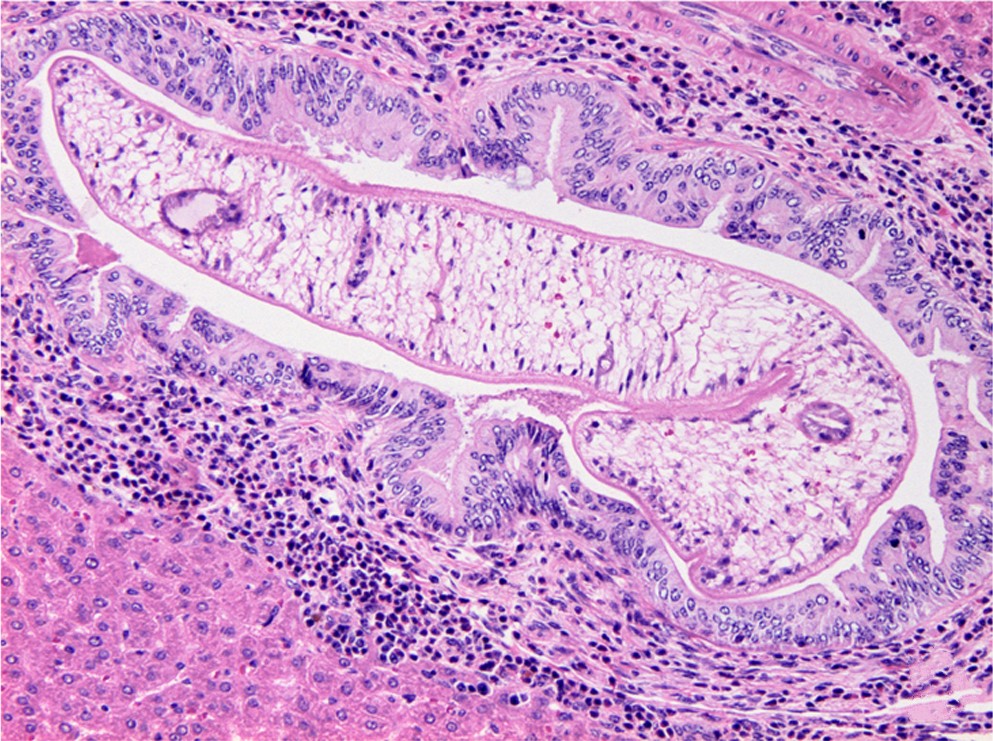
Dos nuevos biomarcadores podrían facilitar un mejor diagnóstico de una infección hepática relacionada con un tipo de cáncer biliar
Un estudio internacional con participación del Centro Nacional de Microbiología (CNM) del Instituto de Salud Carlos III (ISCIII) ha logrado avances que podrían facilitar el diagnóstico rápido de un parásito que afecta al hígado, provocando una infección -opistorquiasis- ligada a un mayor riesgo de desarrollar colangiocarcinoma, un tipo de cáncer de las vías biliares. La investigación se ha publicado en la revista Nature Communications. Opisthorchis viverrini es un parásito hepático de gran importancia, principalmente en regiones del Sudeste Asiático, especialmente en países como Tailandia, Laos y Camboya, y que puede infectar a humanos a través del consumo de pescado crudo o poco cocinado. La opistorquiasis, ligada a altas tasas de mortalidad si no se diagnostica a tiempo, está reconocida por la Organización Mundial de la Salud (OMS) como un carcinógeno biológico del grupo 1, debido a su fuerte asociación con el colangiocarcinoma, un cáncer que afecta a las vías que transportan la bilis desde el hígado al intestino delgado. El objetivo del estudio era desarrollar pruebas diagnósticas rápidas del tipo point-of-care (PoC) para la infección por O. viverrini y colangiocarcinoma asociado. Estas herramientas point-of-care permiten realizar diagnósticos en el mismo sitio de atención al paciente. La investigación está liderada por un equipo internacional de investigadores tailandeses, estadounidenses y australianos, y en ella participa Javier Sotillo, del CNM-ISCIII. El trabajo revela el desarrollo de un microarray proteómico pionero -un chip capaz de analizar material biológico diverso, como los genes- basado en el secretoma del parásito -conjunto de proteínas que desarrollan su función fuera de las células-. Esta herramienta ha permitido evaluar la respuesta de diferentes anticuerpos en sueros de personas infectadas por O. viverrini en Tailandia y Laos, y en pacientes con colangiocarcinoma ligado a la infección. El investigador del CNM-ISCIII ha participado en la recogida, análisis e interpretación de la información derivada del desarrollo del microarray. Gracias a este análisis proteómico, se han identificado nueve antígenos candidatos para la mejora diagnóstica, entre los que destacan una proteasa catepsina tipo C y una enzima IDH-dependiente de la enzima NADP. Ambos candidatos fueron producidos en el laboratorio y aplicados en pruebas inmunocromatográficas rápidas para detectar anticuerpos específicos de la infección, demostrando una mejor sensibilidad y especificidad -por encima del 80%- que los métodos diagnósticos convencionales. Estos dos biomarcadores, según explican los autores, podrían constituir la base para desarrollar nuevas pruebas serodiagnósticas para la infección y el cáncer asociado. Javier Sotillo explica que estas herramientas de diagnóstico rápido y estandarizable "podrían transformar la vigilancia de este parásito hepático en zonas endémicas del Sudeste Asiático, permitiendo detectar tanto infecciones activas como casos de colangiocarcinoma en etapas tempranas, lo que supondría una innovación crucial para mejorar la gestión, control y prevención de esta enfermedad altamente mortal". • Referencia del artículo: Sadaow, L., Rodpai, R., Smout, M.J. et al. Immunomics-guided biomarker discovery for human liver fluke infection and infection-associated cholangiocarcinoma. Nat Commun 16, 5965 (2025). https://doi.org/10.1038/s41467-025-61043-2.
Saber másServicios destacados
Área de Orientación Diagnóstica
Sistema de Respuesta Rápida
Eventos
-
21 may
El viaje de un científico. Del mundo académico a la industria.12:00h.Presencial: Aula 1, Edificio 53, Majadahonda -
07 jun
Sesión científica: ¿Podría la gripe aviar (H5N1) causar una nueva pandemia?18:00h.RANM, c/ Arrieta 12. Madrid
Empleo
SGSAFIPY 318/24-2 M3-1 M1-INDEFINIDO
Inicio de plazo: 11/06/2025
Fin de plazo: 24/06/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
MPY 240/23 -M2-INDEFINIDO
Inicio de plazo: 11/04/2025
Fin de plazo: 29/04/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
MPY 304/24 M1-INDEFINIDO
Inicio de plazo: 09/04/2025
Fin de plazo: 24/04/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)






